某溶液中可能含有Na+、K+、AlO2-、CO32-、SO32-、Cl-中的若干种离子。某同学设计并完成了如下实验: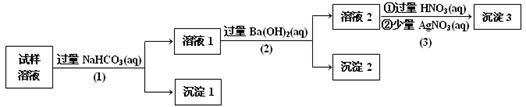
已知:AlO2-+HCO3-+H2O==Al(OH)3+CO32-
根据以上实验操作与现象,该同学得出的结论不正确的是
| A.沉淀2放置在空气中,若质量增加,试样中肯定存在SO32- |
| B.试样溶液中加入稍过量的NH4Cl溶液能得到与沉淀1成分相同的物质 |
| C.上述流程步骤(1)(2)(3)的顺序改为(3)(2)(1),可能会获得相同的实验现象 |
| D.试样溶液中肯定存在AlO2-、Cl-,其中Na+、K+至少存在1种 |
将金属钠分别投入下列物质的溶液中,有气体放出,且溶液质量减轻的是
| A.稀盐酸 | B.K2SO4 | C.CuCl2 | D.NaOH溶液 |
已知水和苯不互相溶,苯不与钠反应,在烧杯中加水和苯(密度:0.88 g/mL)各50 mL。将一小粒金属钠(密度:0.97 g/mL)投入烧杯中,观察到的现象可能是
| A.钠在水层中反应并四处游动 |
| B.钠停留在苯层中不发生反应 |
| C.钠在苯的液面上反应并四处游动 |
| D.钠在苯与水的界面处反应,可能做上下跳动 |
下列有关试剂的保存方法错误的是
| A.少量的钠保存在煤油中 | B.新制的氯水保存在棕色试剂瓶中 |
| C.漂白粉要密闭保存 | D.浓盐酸保存在敞口试剂瓶中即可 |
下列对物质的量理解正确的是
| A.物质的量就是物质的质量 |
| B.物质的量是一种基本物理量 |
| C.物质的量就是物质的摩尔质量 |
| D.物质的量就是物质所含粒子的数量 |
化学科学的特征是
| A.研究物质的变化 | B.制造新物质 |
| C.认识分子和制造分子 | D.做实验 |