【原创】已知25℃时下列酸的电离平衡常数:K(CH3COOH)=1.75×10—5、K(HCN)=6.2×10—10、K1(H2CO3)=4.2×10—7、K2(H2CO3)=5.6×10—11
下列选项不正确的是
| A.过量CO2通入NaCN溶液中:2NaCN+H2O+CO2=2HCN+Na2CO3 |
| B.经测定CH3COONH4的水溶液呈中性可知:K(NH3•H2O)=1.75×10—5 |
| C.将等物质的量浓度的CH3COONa与NaCN溶液等体积混合后的溶液中:c(CH3COO-)>c(CN-) |
| D.常温下将10ml的PH=3的醋酸溶液稀释到100ml,其PH<5 |
化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是()
| A.该反应是吸热反应 |
| B.断裂1mol A—A键和1mol B—B键能放出xkJ的能量 |
| C.断裂2mol A—B键需要吸收ykJ的能量 |
| D.2mol AB的总能量高于1 mol A2和1mol B2的总能量 |
已知1g氢气完全燃烧生成水蒸气时放出121kJ的能量,且氧气中1molO=O键完全断裂时需要吸收496kJ的能量,水蒸气中1mol H—O键形成时放出463kJ的能量,则氢气中1mol H—H键断裂时吸收的能量为()
| A.920kJ | B.557kJ | C.436kJ | D.181kJ |
下列说法正确的是()
| A.任何化学反应都伴随着能量的变化 |
| B.H2O(g)―→H2O(l)的过程放出大量的热,所以该过程是化学变化 |
| C.化学反应中能量的变化都表现为热量的变化 |
| D.如图所示的是吸收能量的过程 |
已知断开1mol H—H键吸收的能量为436kJ,形成1mol H—N键放出的能量为391kJ,根据化学方程式N2+3H2 2NH3,反应完1mol N2放出的能量为92.4kJ,则断开1mol N≡N键需吸收的能量是()
2NH3,反应完1mol N2放出的能量为92.4kJ,则断开1mol N≡N键需吸收的能量是()
| A.431kJ | B.945.6kJ | C.649kJ | D.869kJ |
北京奥运会开幕式在李宁点燃鸟巢主火炬时达到高潮。奥运火炬采用的是环保型燃料——丙烷,其燃烧时发生反应的化学方程式为C3H8+5O2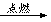 3CO2+4H2O。下列说法中不正确的是()
3CO2+4H2O。下列说法中不正确的是()
| A.火炬燃烧时化学能只转化为热能 |
| B.所有的燃烧反应都会释放热量 |
| C.1mol C3H8和5mol O2所具有的总能量大于3mol CO2和4mol H2O所具有的总能量 |
| D.丙烷完全燃烧的产物对环境无污染,故丙烷为环保型燃料 |