将pH=1的盐酸平均分为两份,一份加适量水,另一份加入与该盐酸物质的量浓度相同的适量NaOH溶液后,pH都升高1,则加入的水与NaOH溶液的体积比为
| A.9 | B.10 | C.11 | D.12 |
对下列实验现象的推测中,正确的是( )
A.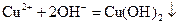 ,将 ,将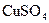 溶液滴入氨水中,振荡,会产生蓝色沉淀 溶液滴入氨水中,振荡,会产生蓝色沉淀 |
B.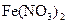 溶液中存在平衡: 溶液中存在平衡: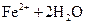 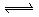  ,加入少量稀盐酸后溶液浅绿色会加深 ,加入少量稀盐酸后溶液浅绿色会加深 |
C. 有漂白性,将 有漂白性,将 通入石蕊试液中,溶液将先变红后褪色 通入石蕊试液中,溶液将先变红后褪色 |
| D.硫酸铝溶液显酸性,次氯酸钠溶液显碱性,这两种溶液混合后会产生白色沉淀 |
一支25mL的酸式滴定管注入0.10mol/L盐酸溶液后,液面正好在5mL刻度处.则滴定管内盐酸溶液的体积为( )
| A.等于5mL | B.大于5mL,小于20mL |
| C.等于20mL | D.大于20mL |
微量元素是指人体内总含量不到万分之一,重量总和不到人体重量的千分之一的20多种元素,这些元素对于人体的正常发育和健康起着重要作用,下列各组元素全部都是微量元素是( )
| A.Na、K、Cl、S、O | B.F、I、Fe、Zn、Cu |
| C.N、H、O、P、C | D.Ge、Se、Cu、Mg、C |
下列说法中正确的是()
| A. | 全部由极性键构成的分子一定是极性分子 |
| B. | 非极性分子中一定没有极性键 |
| C. | 离子晶体中一定没有共价键 |
| D. | 分子晶体中一定没有离子键 |
20 由两种金属粉末组成的混合物,与足量的盐酸充分反应后得到11.2 氢气(标准状况),这种金属混合物的组成可能是
| A. | 和 | B. | 和 |
| C. | 和 | D. | 和 |