已知:3NO3-+8Al+5OH-+2H2O 3NH3↑+8AlO2—。某地区的雾霾中可能含有如下可溶性离子:Na+、NH4+、Mg2+、Al3+、SO42—、NO3—、HCO3—、Cl-。某同学收集了该地区的雾霾,经必要的预处理后试样溶液,设计并完成如下实验:
3NH3↑+8AlO2—。某地区的雾霾中可能含有如下可溶性离子:Na+、NH4+、Mg2+、Al3+、SO42—、NO3—、HCO3—、Cl-。某同学收集了该地区的雾霾,经必要的预处理后试样溶液,设计并完成如下实验: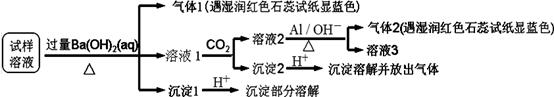
根据以上的实验操作与现象,该同学得出的结论错误的是
| A.试样中肯定存在NH4+、SO42—和NO3—,可能有Mg2+ |
| B.试样中不一定存在Na+、Cl-、HCO3— |
| C.沉淀2中可能含碳酸钡、碳酸镁和氢氧化铝 |
| D.该雾霾中可能存在NaNO3、NH4HCO3和MgSO4 |
用石墨电极电解100mL H2SO4与CuSO4的混合液,通电一段时间后,两极均收集到2.24L(标况)气体,则原混合液中Cu2+的物质的量浓度为
| A.0.5mol/L | B.1mol/L | C.2mol/L | D.4mol/L |
白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P="O" ckJ·mol—1、O=O dkJ·mol—1。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
| A.(6a+5d-4c-12b)kJ·mol—1 | B.(4c+12b-6a-5d)kJ·mol—1 |
| C.(4c+12b-4a-5d)kJ·mol—1 | D.(4a+5d-4c-12b)kJ·mol—1 |
Fe2O3(s)+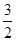 C(s)===
C(s)===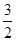 CO2(g)+2Fe(s) ΔH1=+234.1 kJ/mol;C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol;则2Fe(s)+
CO2(g)+2Fe(s) ΔH1=+234.1 kJ/mol;C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol;则2Fe(s)+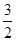 O2(g)===Fe2O3(s)的ΔH是
O2(g)===Fe2O3(s)的ΔH是
| A.-627.6 kJ/mol | B.-824.4 kJ/mol |
| C.-744.7 kJ/mol | D.-169.4 kJ/mol |
下列反应属于吸热反应的是
①二氧化碳与赤热的炭反应生成一氧化碳
②液态水汽化
③锌粒与稀H2SO4反应制取H2
④Ba(OH)2·8H2O固体与NH4Cl固体反应
⑤生石灰跟水反应
| A.①②④ | B.①⑤ | C.①③④⑤ | D.①④ |
一个原电池的总反应方程式为Zn+Cu2+===Zn2++Cu,该原电池可能为
| A |
B |
C |
D |
|
| 正极 |
Cu |
Al |
Zn |
Fe |
| 负极 |
Zn |
Zn |
Cu |
Zn |
| 电解质溶液 |
H2SO4 |
CuSO4 |
ZnCl2 |
CuCl2 |