(12分)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察下图,然后回答问题。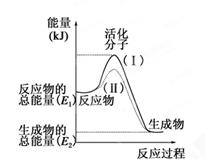
(1)图中所示反应是________(填“吸热”或“放热”)反应。
(2)已知拆开1mol H—H键、1mol I—I、1mol H—I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由1mol氢气和1mol 碘反应生成HI会________(填“放出”或“吸收”)________kJ的热量。在化学反应过程中,是将___ ___转化为________。
(3)50mL 0.50mol•L﹣1盐酸与50mL 0.55mol•L﹣1 NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中的热量可计算中和热.回答下列问题: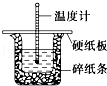
①从实验装置上看,图中尚缺少的一种玻璃用品是 .
②烧杯间填满碎纸条的作用是 .
③大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”、“偏小”或“无影响”).
④实验中改用60mL 0.50mol•L﹣1盐酸跟50 mL 0.55mol•L﹣1 NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”),简述理由: 。
⑤用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会 (均填“偏大”、“偏小”或“无影响”)
X、Y、Z、W、Q、R均为前4周期元素,且原子序数依次增大。其相关信息如表所示:
| X元素的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同 |
| Y原子的2p轨道中有3个未成对电子 |
| Z元素的族序数是其周期数的3倍 |
| W原子的第一至第四电离能分别为: I1=578 kJ·mol-1I2=1 817 kJ·mol-1I3=2 745 kJ·mol-1 I4=11 575 kJ·mol-1 |
| Q为前4周期中电负性最小的元素 |
| 元素R位于周期表的第11列 |
请回答下列问题:
(1)Y3-的原子结构示意图为___________________,Y的氢化物的空间构型为______________。
快速制备Y的氢化物可用Y的氢化物的浓溶液与NaOH固体的原因_________________。
(2)已知YZ2+与XZ2互为等电子体,写出YZ2+的电子式____________________。
(3)R的基态原子价电子排布式为______________________,R的氯化物的水溶液与Q单质发生反应的离子方程式为____________________________________________________。
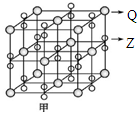
(4)化合物甲由Z、Q两种元素组成,其晶胞如图,甲的化学式为
________________。
(5)已知由X形成的自然界硬度最大的单质完全燃烧的燃烧热
为395 kJ/mol。且1 mol Z=Z键完全断裂时吸收热量497 kJ,1 mol
X=Z键形成时放出热量745 kJ,则单质X中1 mol X—X键断裂时吸收热量为___________________。
(16分)实验室需要80mL 2mol/L碳酸钠溶液。回答下列有关配制该溶液的问题(实验室中没有80mL规格的容量瓶):
(1)所需要的仪器为:托盘天平、量筒、烧杯、玻璃棒、_________、_________。
(2)配制该溶液需要Na2CO3的质量为_________g。
(3)配制溶液的操作顺序是(填序号)_________。
①转移溶液;②轻摇使溶液混合均匀; ③洗涤并转移洗涤液;④加盖倒转摇匀溶液; ⑤定容; ⑥称量⑦溶解;⑧计算
(4)正式配制前必须进行的一项实验操作是__________________。
(5)试分析下列操作对所配溶液的浓度有何影响:(填写编号)
A.偏高;B.不变;C.偏低。
①配制溶液时未洗涤烧杯并转移洗涤液_________;
②定容、加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线_________;
③定容时俯视刻度线_________。
一学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物
填空和回答下列问题
(1)B物质是(写化学式)
(2)按此实验方案分离得到的NaCl,经分析含有杂质,此杂质的化学式为,因为上述方案中某一步设计有毛病,这一步的正确设计方案应是。
(3)写出生成沉淀B的离子方程式
(4)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是
下图中A~H均为中学化学中常见的物质。已知A为紫红色金属,D能使品红溶液褪色,E为生活中常见的无色无味液体,F为黄绿色气体。请回答下列问题: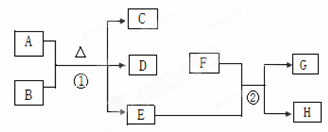
(1)反应②中能起杀菌消毒作用的化合物是(填名称)
(2)反应①的化学方程式为。
(3)D物质造成的环境问题是,实验室常用过量的NaOH溶液来吸收它,该反应的离子方程式为
(4)待A(足量)与B反应停止后,反应混合液中的B仍有剩余。其原因是。
A~K为中学化学的常见物质,它们之间有如下图所示的转化关系(反应条件已略去)。已知:通常状况下,A是淡黄色固体,B、D和I都是无色气体单质,F是红棕色气体,H是金属单质。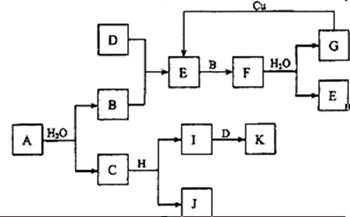
回答下列问题:
(1)写出化学式A______,F_______,G_______,H_______,J________,K________,。
(2)写出实验室制取K的化学方程式__________________________________________。
(3)写出G→E的化学方程式_________________________________________________;
此反应中,氧化剂和还原剂的物质的量之比是_____________;
0.3mol Cu完全反应,被还原的G为_____________mol。
(4)检验C中阳离子的实验方法是____________________________________________。
(5)实验室中保存的C溶液可能会变质,为了检验C溶液是否变质,分别取少量样品进行如下实验,其中能达到实验目的的是__________(填序号)。
a.向样品中滴加稀硝酸,观察现象
b.向样品中滴加氢氧化钡溶液,观察现象
c.向样品中滴加酚酞试液,观察现象
d.向样品中滴加氯化镁溶液,观察现象