(9分)实验室制备溴苯可用下图所示装置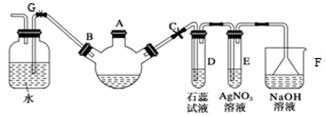
填空:
(1)关闭G夹,打开C夹,向装有少量苯的三颈烧瓶的A口加少量溴,再加入少量铁屑,塞住A口,三颈烧瓶中发生反应的化学方程式为 。
(2)D、E试管内出现的现象依次为 、 。
(3)F装置的作用是 。
(4)待三颈烧瓶中的反应进行到仍有气泡冒出时松开G夹,关闭C夹,可以看到的现象是 。
(5)反应结束后,拆开装置,从A口加入适量的NaOH溶液,目的是 ,然后将液体倒入 (填仪器名称)中,振荡静置,从该仪器 口(填“上”或“下”)将溴苯放出。
实验室配制500mL 0.1mol/L的NaOH溶液,有如下操作步骤:
①计算所需NaOH固体的质量并用托盘天平称取;
②将称量好的NaOH固体放入烧杯中,加入适量的蒸馏水溶解;
③用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶中并轻轻摇匀;
④继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,小心滴加蒸馏水至溶液凹液面与刻度线相切;
⑤塞紧容量瓶的塞子,充分摇匀。
回答下列问题:
(1)本实验中除用到容量瓶和烧杯外,还需要用到的玻璃仪器有:
。
(2)实验中用托盘天平实际称取NaOH固体的质量是。
(3)上述实验操作步骤缺少一步,请补充所缺步骤的位置及内容:
。
(4)在实验中,未进行操作④,所配溶液的浓度会(填“偏高”、“偏低”或“无影响”,下同);
定容时俯视液面,所配溶液的浓度会。
称量时已观察到NaOH吸水,所配溶液的浓度会。
(16分)双安妥明是一种降血脂药物,主要用于降低血液中胆固醇浓度,安全,副作用小,其结构简式为:
已知:
双安妥明的合成路线如下:
已知:C的摩尔质量是同温同压下氢气质量的28倍;I能发生银镜反应且1mol I能与2molH2S生加成反应;K的结构具有对称性。试回答下列问题:
(1)双安妥明的分子式为:_____________。
(2)E的结构简式为:________________________
(3)反应②的条件是__________________
(4)J与新制氢氧化铜发生反应的化学方程式为:__________________
(5)反应④的化学方程式为:______________________________
(6)符合下列3个备件的H的同分异构体有____________种,①能与FeCl3溶液显色;②苹环上只有2个取代基:③1mol该物质最多可消耗3mol NaOH,其中氢原子共有五种不同环境的是(写结构筒式)____________
(14分) 在工业生产和日常生活中有重要用途。 I.工业上用钛矿石(
在工业生产和日常生活中有重要用途。 I.工业上用钛矿石( ,含
,含 等杂质)经过下述反应制得:
等杂质)经过下述反应制得:
其中,步骤②发生的反应为: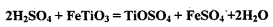
(1)净化钛矿石时,是否需要除去杂质FeO? ______ (填“需要”或“不需要”)。
(2)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式: __________________
II. TiO2可通过下述两种方法制备金属钛:
“方法一”是电解TiO2来获得Th将处理过的TiO2作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池。
(3)阴极反应的电极反应式为__________________
“方法二”是先将TiO2与 Cl2、C反应得到TiCl4,再用镁还原得到TL因下述反应难于发生:
所以不能直接由Ti02和Cl2反应(即氯化反应)来制取TiCl4。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
(4)己知:
请写出 与Cl2、C反应制取TiO4的热化学方程式:____________
与Cl2、C反应制取TiO4的热化学方程式:____________
(5)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因________________________________________________
(16分)测定化成SO3的转化率可以用题27—1图装置,装置中烧瓶内发生的化学反应方程式为: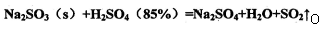
(已知S03的熔点是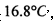 沸点是
沸点是 )
)
(1)装置中甲管的作用是__________________。
(2)根据实验需要,应该在I、II、III、IV处连接合适的装置,请从题27〜2图A〜E装置中选择最适合装置并将其序号填放下面的空格中。
I、 II、III、IV处连接的装置分别是________________________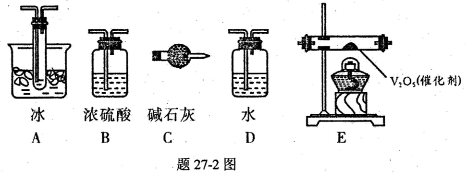
(3)为使SO2有较高的转化率,实验中加热fi化剂与滴加浓硫酸的顺序中,应采取的操作是______________________________ ,若用大火加热烧瓶时,SO2的转化率会____________ (填“升高”、“不变”或“降低”)。
(4)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因(可以不填满)
①原因:______②原因:______ ③原因:______
(5)将SO2通入含1mol氯酸的溶液中,可生成一种强酸和一种氧化物,并有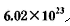 个电子转移,则该反应的化学方程式为__________________
个电子转移,则该反应的化学方程式为__________________
(6)用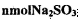 粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2 —段时间后,测得装置IV增重了 mg,则实验中SO2的转化率为__________________.(用含m、n的代数式填写)
粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2 —段时间后,测得装置IV增重了 mg,则实验中SO2的转化率为__________________.(用含m、n的代数式填写)
某研究性学习小组成员分别设计了如下甲、乙、丙三套实验装置制取乙酸乙酯。请 回答下列问题:
回答下列问题:
(1)A试管中的液态物质有。
(2)甲、乙、丙三套装置中,不宜选用的装置是。(选填“甲”、“乙”、“丙”)
(3)写出试管A中发生的化学反应方程式 。
。