某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl,AgBr,AgI的Ksp依次减小。已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX—pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系。下列说法错误的是
| A.e点表示由过量的KI与AgNO3反应产生AgI沉淀 |
| B.A线是AgCl的溶解平衡曲线,C线是AgI的溶解平衡曲线 |
| C.d点是在水中加入足量的AgBr形成的饱和溶液 |
| D.坐标点(8,4)形成的溶液是AgCl的不饱和溶液 |
下列有机物的命名正确的是()
A. 2—甲基—3—丁烯 2—甲基—3—丁烯 |
B.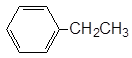 乙基苯 乙基苯 |
C.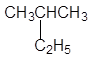 2—乙基丙烷 2—乙基丙烷 |
D.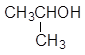 1—甲基乙醇 1—甲基乙醇 |
氯仿(CHCl3)可以作为麻醉剂,常因保管不善被空气氧化,生成剧毒物质光气(COCl2):2CHCl3+O2→2HCl+2COCl2,为防止出现医疗事故,使用前要检验其是否变质,应选用的试剂是()
| A.NaOH溶液 | B.溴水 | C.酚酞试液 | D.AgNO3 |
实验室中,下列除去括号内杂质的有关操作正确的是 ( )
| A.苯(硝基苯):加少量水振荡,待分层后分液 |
| B.乙醇(水):加新制生石灰,蒸馏 |
| C.CO2(HCl、水蒸气):通过盛有碱石灰的干燥管 |
| D.乙烷(乙烯):催化加氢 |
某有机物H3C—CH=CH—COOH,不能发生的反应类型()
| A.氧化反应 | B.加成反应 | C.酯化反应 | D.水解反应 |
下列说法错误的是()
| A.乙醇和乙酸都是常用调味品的主要成分 |
| B.乙醇、乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高 |
| C.乙醇和乙酸都能酸性高锰酸钾溶液褪色 |
| D.乙醇和乙酸之间能发生酯化反应,酯化反应为可逆反应 |