实验是研究物质的性质及其变化规律的重要手段,请根据下述实验内容回答问题。
小资料:
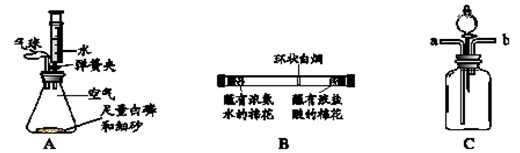
1.白磷的着火点为40℃。
2.浓盐酸和浓氨水均是具有挥发性的无色液体,挥发出的氯化氢气体和氨气反应生成氯化铵。
(1)图A为测定空气中氧气含量的实验。锥形瓶内空气体积为220mL,注射器中水的体积为50mL,实验时先夹紧弹簧夹,将锥形瓶底部放入热水中,白磷很快被引燃,白磷燃烧的化学方程式为 。将锥形瓶从热水中取出,待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,可观察到的现象是 。
(2)图B为探究分子运动的实验,在玻璃管两端同时放入蘸有试剂的棉花,发现在玻璃管内形成了环状白烟且偏向蘸有浓盐酸的棉花一端。由此得到的结论是 。
(3)在验证二氧化碳与水反应实验中,为证明使石蕊变色的物质是碳酸而不是水或二氧化碳,使用如图C所示的装置,应采取的实验操作顺序是 (填数字序号,可重复选用)。
①从b端通氮气;②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中;③从a端通二氧化碳;④从分液漏斗中滴加适量水
我国古代将炉甘石、赤铜和木炭粉混合加强热,制得外观似金子的黄铜(铜锌合金),现取一定量含少量木炭粉的黄铜粉末样品,测定其中铜、锌的质量比,设计如下实验流程和装置。

(1)气体X是 ,步骤I的目的是: 。
(2)步骤II中,若通过测定铜的质量来确定黄铜中铜、锌的质量比,简述从黄铜中分离出铜的实验操作。
(3)步骤II中,若不测定铜的质量,某同学认为,结合图提供的装置进行实验,即使装置气密性不良,也能达到实验目的,写出实验过程中需要测量的数据。
在实验室利用以下装置进行气体的制取和性质实验。
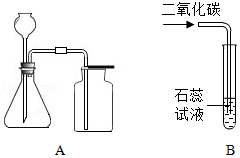
(1)用装置A制取氧气、二氧化碳的化学方程式分别为: 、 ,发生装置相同的理由是: ,收集气体的方法是: 。
(2)装置B观察到的现象是: ,反应的化学方程式为 。
碳酸钠在生活和生产中都有广泛的用途。为探究碳酸钠的化学性质,同学们做了如下实验。

请根据实验回答问题。
(1)A试管中溶液变成红色,说明碳酸钠溶液显 性。
(2)B试管中观察到的实验现象为 ,说明碳酸钠能与盐酸反应。
(3)C试管中有白色沉淀产生,写出该反应的化学方程式 。实验结束后,同学们将三支试管中的物质倒入同一个洁净的烧杯中,静置段时间后,观察到烧杯底部有白色沉淀,上层溶液为无色。
【提出问题】无色溶液中除酚酞外还有哪些溶质?
【分析讨论】无色溶液中定含有的溶质是 (填化学式,下同);可能含有的溶质是 。
【实验验证】为检验无色溶液中可能含有的溶质是否存在,请你帮助他们设计实验方案 (写出实验操作、现象及结论)。
在一次化学课上,老师提供了以下装置制取二氧化碳并验证其性质。请回答。

(1)仪器a的名称是 。
(2)实验室制取二氧化碳的反应原理是 (用化学方程式表示)。实验室常用A装置作为制取二氧化碳的发生装置,选择气体发生装置时,应考虑的因素有 ;收集二氧化碳应选择的装置是 (填字母序号)。
(3)收集到的二氧化碳中常混有氯化氢气体。要除去二氧化碳中混有的氯化氢,将气体通过E装置能否达到实验目的? (填“能”或“否”)。
(4)用F装置验证二氧化碳的性质,通入二氧化碳后,试管中产生的现象是 。
某化学兴趣小组做粗盐中难溶性杂质去除的实验,实验过程如图所示。
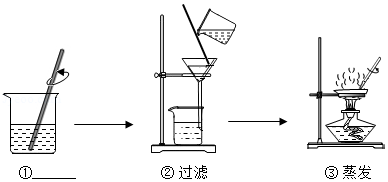
(1)步骤①的名称是 。
(2)步骤②中,玻璃棒的作用是 。
(3)步骤③中,当观察到蒸发皿内出现 时,停止加热。
(4)将氯化钠与泥沙分离所采用的方法,利用了氯化钠具有 的性质。