金属的冶炼与回收使资源得到了充分利用。
①火法炼铁的原理是Fe2O3+3CO 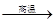 2Fe +3CO2,实验室现有不纯的CO(混有CO2和水蒸气),若要用纯净、干燥的一氧化碳还原氧化铁并检验生成的气体,下述装置的正确连接顺序为(假设每步均完全反应,装置不得重复使用):不纯的CO→( 27 ) (填字母)。
2Fe +3CO2,实验室现有不纯的CO(混有CO2和水蒸气),若要用纯净、干燥的一氧化碳还原氧化铁并检验生成的气体,下述装置的正确连接顺序为(假设每步均完全反应,装置不得重复使用):不纯的CO→( 27 ) (填字母)。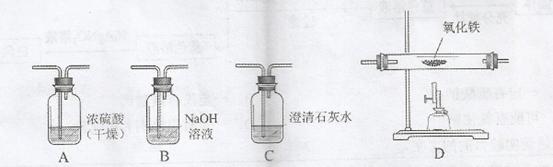
②湿法炼铜的原理是用稀硫酸将矿石中的氧化铜溶解,然后用较活泼的金属置换出铜。将0.2mol铁粉放入足量硫酸铜溶液中,理论上能生成(28)g铜(根据化学方程式计算)
③现欲从含有CuSO4的废液中回收铜,同时得到工业原料——硫酸亚铁晶体。设计方案如下: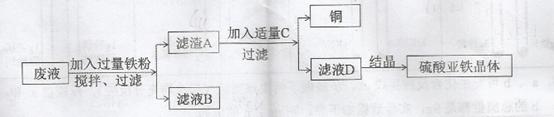
I.滤渣A的成分是( 29) ,C物质是( 30) 。
II.从提高硫酸亚铁晶体回收率的角度分析,该方案的一个不足之处是( 31) 。
④上述铜的冶炼和回收过程中,铜元素存在形态的变化是( 32) 。
A.游离态→化合态 B.化合态→游离态
碳及碳的化合物在人类生产生活中应用广泛,随着科技的不断涌现。请根据所学知识回答下列问题:
(1)下列含碳元素的物质中,属于有机物的是(填字母序号)。
A.碳酸钙 B.乙醇 (
) C.一氧化碳
(2)如图"碳海绵"是已知最轻的固体材料,只由碳元素组成,具有多孔结 构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法不正确的是(填字母序号)。
A.具有吸附性 B.可重复使用C.可处理海上泄露的石油 D.属于复合材料
(3)倡导"低碳"生活,主要是为了减少(填化学式)的排放量。请举一例在日常生活中符合这一主题的做法。
用化学用语填空:
(1)2个氮原子
(2)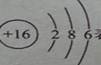 表示的原子结构示意图
表示的原子结构示意图
(3)地壳中含量最多的金属元素。
(1)实验室可用草酸(
)在浓硫酸的作用下分解制得一氧化碳和二氧化碳(化学方程式为:
↑
↑)。用到的实验装置见下图:
若分别得到一氧化碳和二氧化碳,请回答:
①装置
中,盛放浓硫酸的仪器名称是;
②收集一氧化碳时,打开
、
,关闭
,装置
的作用是。由于一氧化碳有毒,多余的气体应(填写具体处理办法);
③关闭、打开,释放出二氧化碳,并通过装置可收集到干燥的二氧化碳气体。
(2)在二氧化锰的催化作用下,过氧化氢迅速分解生成氧气和水。哪些因素还影响着过氧化氢分解的速率?课外活动小组结些进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
| 实验步骤 |
现象 |
结论 |
| 取一支试管加入
5%的过氧化氢溶液,然后加入少量二氧化锰。 |
缓慢有少量气泡冒出 |
|
| 另取一支试管加入
15%的过氧化氢溶液,然后加入少量二氧化锰。 |
迅速有大量气泡冒出 |
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
| 实验步骤 |
现象 |
结论 |
| 温度越高,过氧化氢分解的速率越大 |
||
近年,我国不少城市和地区雾霾天气增多,雾是水蒸气,本身无污染,"霾"由细小颗粒物组成,主要来源是热电排放、化工生产、汽车尾气、冬季供暖以及地面灰尘等。它侵蚀着人们的健康,严重影响着人们的生活和出行。下面治理雾霾的措施中,可行的是。
①压减化石燃料 ②控制车辆使用 ③减少户外运动
④加强城市绿化 ⑤关闭厂矿企业 ⑥调整能源结构
用滤纸折成蝴蝶并喷洒某种溶液或试剂后,悬挂于铁架台上。另取一只盛有某未知溶液的烧杯,放在纸蝴蝶的下方(见下图)。一会儿,纸蝴蝶的颜色发生变化,请回答: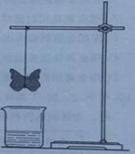
(1)若纸蝴蝶上喷洒的是酚酞试液,纸蝴蝶变红色,烧杯中的溶液是;
(2)若纸蝴蝶上喷洒的是石蕊试液,纸蝴蝶变红色,烧杯中的溶液是,
若纸蝴蝶变蓝色,烧杯中的溶液是;
(3)试分析产生以上现象的原因是。