甲、乙两种物质的溶解度曲线如图所示。
(1)甲、乙两种物质中,溶解度受温度影响较大的是 物质。
(2)t2℃时,甲、乙两种物质各70g分别加入100g水中,能形成饱和溶液的是 物质。
(3)若甲物质中混有少量的乙物质,提纯甲物质可采取的方法是 (填“降温结晶”或“蒸发结晶”)。
(4)将t1℃时甲、乙的饱和溶液升温到t2℃,所得溶液的溶质质量分数的关系是:甲 乙(填“>”、“=”或“<”)。
下图是实验室常用的制取气体的发生装置和收集装置,根据实验装置,回答有关问题: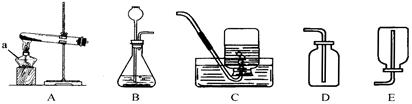
(1)仪器a的名称是______。
(2)在我们学过的实验室制取气体的方案中,有一种气体可以选用B装置制备,D装置收集,但不宜选用C装置收集,则该气体的化学式是____ _ _,
实验室制备该气体的化学方程式为______。
(3)在我们学过的实验室制取气体的方案中,有一种气体既可以用A装置制取,也可以用B装置制取,该气体的化学式是______,下面是用A、C装置制取这种气体的实验报告,请你填写完整。
| 操作步骤 |
现象 |
结论或解释 |
①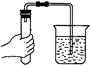 |
导气管口有气泡冒出,松开手后有一小段水柱上升 |
这说明:_______________; |
② 加入高锰酸钾 |
||
③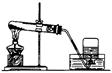 |
导气管口有气泡产生 |
反应的化学方程式为_______ ; |
| ④以下两步的操作顺序是_ __ A.熄灭酒精灯 B.取出导气管 |
按此顺序操作的目的是 ___________________。 |
通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下: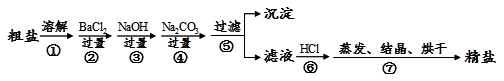
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是。
(2)第②步操作加入过量的BaCl2目的是除去粗盐中的(填化学式),
写出这个反应的化学方程式。
(3)第⑤步“过滤”操作中得到沉淀的成分有:
泥沙、BaSO4、CaCO3、BaCO3(填化学式)。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,
理由是。
(5)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是______。
下图是常见固体物质的溶解度曲线,根据图示回答: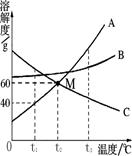
(1)曲线上M点表示,
t3℃时,A、B、C三种物质的溶解度由大到小的顺序为。
(2)t1℃时,将10g A物质放入100g水中,充分溶解后所得的溶液是(填“饱和”或“不饱和”)溶液。
欲使t2℃时C物质的饱和溶液变为不饱和溶液,可采取的方法是_____________(任填一种方法)。
(3)现有30℃的不饱和KNO3溶液,与该溶液有关的量有:①水的质量 ②溶液中KNO3的质量 ③KNO3的质量分数 ④30℃时KNO3的溶解度 ⑤溶液的质量
Ⅰ.在该不饱和溶液中加硝酸钾至饱和,不变的量有(填序号,下同)。
Ⅱ.将该不饱和溶液恒温蒸发至饱和,不变的量有
空气、水、燃料是人类赖以生存的自然资源。
(1)人类时刻都离不开空气,是因为空气中的氧气能
(2)为了保护环境,用煤作燃料的煤炉要适当增加进风口,将煤粉吹起使之剧烈燃烧,请解释这种做法能使煤完全燃烧的原因是,若要达到低碳减排的目的,下列措施不可行的是。
| A.改变燃料结构 | B.开发新能源 |
| C.减少化石燃料使用 | D.将排出的二氧化碳压缩液化埋入深海中 |
(3)自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:
图乙所示反应的基本类型为;
写出图甲所示反应的化学方程式 。
(1)酸雨是天空降水呈酸性(pH小于5.6)的统称,形成硫酸型酸雨的主要物质的化学式为 ;
(2)酸雨可导致的危害有(填编号).
| A.腐蚀建筑物 | B.导致树木枯萎 | C.造成洪涝灾害 | D.影响农作物生长 |