汽车、电动车一般使用铅酸蓄电池。某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸。
(1)若用50 g质量分数为98%的浓硫酸配制该稀硫酸时,用量筒量取水 mL(水的密度可看作为1 g/cm3)。
(2)在实验室用浓硫酸配制稀硫酸的主要步骤有:计算、量取、 、装瓶并贴上标签。
(3)为了实验的安全,在稀释时应将 沿容器壁慢慢倒入 中,并用玻璃棒不断搅拌。若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后再涂上3%~5%的 溶液。
(4)用配制的硫酸溶液与氢氧化钠溶液反应,实验过程中溶液的pH变化曲线如图所示:A点对应的溶液
呈 (填“酸性”、“碱性”或“中性”);C点对应的溶液中的溶质为 (写化学式)。
“水是生命之源”。请回答下列与水有关的问题:
(1)鱼类可以在水中呼吸,是因为水中溶有______________。
(2)水体污染的来源主要有工业污染、农业污染、____________。
(3)蔗糖在热水中溶解比在冷水中快,用分子的相关知识解释原因是_____________________________。
下表为元素周期表中某一周期元素的原子结构示意图。
| 元素名称 |
钠 |
镁 |
铝 |
硅 |
| 元素符号 |
Na |
Mg |
Al |
Si |
| 原子结构示意图 |
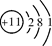 |
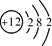 |
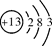 |
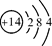 |
| 元素名称 |
磷 |
硫 |
氯 |
氩 |
| 元素符号 |
P |
S |
Cl |
Ar |
| 原子结构示意图 |
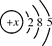 |
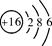 |
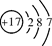 |
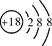 |
请回答下列问题:
(1)表中磷原子的核电荷数x=________。
(2)表中具有相对稳定结构的元素是________。
(3)在化学反应中,每个铝原子失去________个电子形成铝离子。
(4)上述元素在周期表中处于同一周期的原因是__________________。
下表列出了四种金属元素的原子结构及单质的性质等具体情况:
| 元素 名称 |
元素 符号 |
原子结构示意图 |
密度 /g·cm-3 |
熔点 /℃ |
沸点 /℃ |
与冷水 反应 |
| 锂 |
Li |
 |
0.534 |
180.5 |
1 347 |
剧烈 |
| 钠 |
Na |
 |
0.97 |
97.81 |
882.9 |
剧烈 |
| 钾 |
K |
 |
0.86 |
63.65 |
774 |
剧烈 轻微 爆炸 |
| 铷 |
Rb |
 |
1.532 |
38.39 |
688 |
剧烈 轻微 爆炸 |
根据以上资料分析,你发现了哪些规律?
(1)________________________________________________________________________;
(2)________________________________________________________________________;
(3)________________________________________________________________________;
(4)上表所列规律中,有一种规律是决定其他规律的,该规律是:_____________________。
化学从宏观和微观两个角度认识物质。
(1)图甲是两种元素在元素周期表中的信息,图乙是钠原子和氧原子的原子结构示意图。

图甲的横线上填的是________,图乙横线上的数字是________。
(2)某原子的结构示意图如下图所示。回答问题:
该原子核电荷数是________,核外电子层数有________层,电子总数为________个,最外层有电子数________个,在化学反应中易________(填“失”或“得”)电子,成________(填“阳”或“阴”)离子。
元素周期表是学习和研究化学的重要工具。下图是元素周期表的一部分。
(1)查出碳的相对原子质量为________,原子序数为17的元素符号为________。
(2)表中不同种元素最本质的区别是________________________________。