某化学课题小组的同学在学习完了酸、碱、盐后想探究它们之间的性质,他们来到实验室,发现一瓶久置的“碱石灰”(碱石灰的成分是CaO和NaOH的混合物),于是他们进行了如图所示的探究。
【提出问题】:滤液C中的溶质是什么?
【猜想与假设】:小龙同学认为溶质是NaOH,小江同学认为溶质是Na2CO3,小美同学认为溶质是NaOH、Na2CO3,你认为溶质是 ;
【过程与评价】:
(1)小江同学为了证明自己的猜想,取滤液C少许于试管中,滴加足量的稀盐酸,产生大量气泡,则滤液C中溶质是Na2CO3,写出该反应的化学方程式________________小江同学的评价是否正确?原因是什么————--;
(2)小美同学为了证明自己的猜想,取滤液C少许于试管中,滴加少量的CaCl2溶液,产生白色沉淀,写出该反应的化学方程式_____________.静置,向上层清夜中滴加无色酚酞溶液,无色酚酞溶液变红,则滤液C中的溶质为NaOH和Na2CO3,小美同学的实验结论是否正确?原因是什么?_________________
(3)经过同学们的实验证明,小江同学的猜想是错误的,则滤液C中的溶质是______实验过程中,同学们还发现向样品中加入足量的水溶解时放出大量的热,综合对滤液和滤渣成分的探究,下列对样品成分的分析正确的是______
①样品中一定含有NaOH ②样品中一定含有Na2CO3 ③样品中含有NaOH、CaO中的一种或两种
(10分)某校研究性学习小组用右图装置进行镁条在空气中燃烧的实验:将镁条燃烧、冷却后打开止水夹。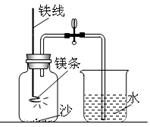
【发现问题】
进入集气瓶中水的体积约占集气瓶容积的30%。如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积应不超过其容积的%。可现进入集气瓶中水的体积约为其容积的30%,根据空气的组成,可推出减少的气体中一定有氮气,这种推测的理由是
。剩余约70%的气体主要成份是。
【提出假设】镁条能与空气中的氮气发生化学反应。
【探究实验】
接着上述实验,先拿开装置中集气瓶的胶塞,然后迅速把点燃的镁条伸进含有剩余气体的集气瓶中。发现镁条能在余下的气体中剧烈燃烧。
【实验结论】根据上述探究实验,你得的结论是。
【查阅资料】
①镁条在氮气中能燃烧并生成氮化镁(Mg3N2)固体。根据资料,氮化镁中氮元素的化合价,该反应的化学方程。
②镁条除了能与氮气反应,还可以在二氧化碳气体中燃烧生成碳和氧化镁。请你写出该反应的化学方程式。
【实验反思】通过以上探究,你对燃烧有了什么新的认识:
。(写出一点即可)。
(12分) 现有下列A、B、C、D、E五种实验装置,根据题意,将装置的序号填入下列空格中。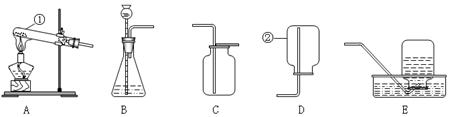
(1)写出指定仪器的名称:①;② 。
(2)用高锰酸钾制取氧气,气体发生装置选用(填序号);用高锰酸钾制取氧气的化学方程式为;
(3)用C装置收集CO2时,检验CO2是否收集满的方法是。
(4)用过氧化氢溶液制取氧气,气体发生装置选用(填序号);用过氧化氢溶液制取氧气的化学方程式为。
(5)氨气(NH3)无色、有刺激性气味,极易溶于水,密度比空气小;实验室常用加热固体硫酸铵和固体氢氧化钙的混合物来制取氨气(在制得氨气的同时还生成了硫酸钙和水)。则氨气的制取和收集的装置是(填序号); 请你写出该反应的化学方程式。
市售某品牌饮料的罐体是A1—Fe合金,为测定其中Al的质量分数,某学习小组精确称取0.050 g合金样品,设计了如下装置并进行实验: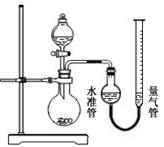
【查阅资料】:1、Al和NaOH溶液反应,放热并生成H2,反应中对应关系为2Al ~ 3H2,Fe和NaOH溶液不反应;2、实验条件下,H2的密度近似为0.090 g·L—1。
【实验步骤】:
①;②装入药品和水,连接装置;③记录量气管中水面读数为5 mL;④打开分液漏斗活塞,逐滴滴入NaOH溶液,至不再产生气泡为止,关闭活塞;⑤待温度降至室温时,记录量气管中水面读数为49 mL;⑥处理剩余药品,整理实验台。
【实验分析及数据处理】:
(1)完善实验步骤中的所缺部分;
(2)检查气密性的方法:打开分液漏斗活塞,向量气管中加入水,使水准管和量气管中水面相平,关闭活塞,降低量气管,若两侧水面高度差(填“改变”或“不变”),则气密性良好;
(3)实验结束后,读取量气管中水面刻度之前,需进行的操作是;
(4)计算此A1—Fe合金样品中Al的质量分数(3分,精确到小数点后3位);;
【实验反思】:
(5)造成实验结果偏大的原因可能是。
A.实验过程加入NaOH溶液的体积
B.没有冷却至室温就开始读数
C.装置漏气
利用铝土矿(只考虑含Al2O3及Fe2O3)生产Al的工艺流程如下,请回答下列问题:
【查阅资料】:1、铝土矿中Al2O3可以和NaOH溶液反应,反应的化学方程式为:
Al2O3 + 2NaOH ="=" 2NaAlO2 + 2H2O;2、Fe2O3不和NaOH溶液反应。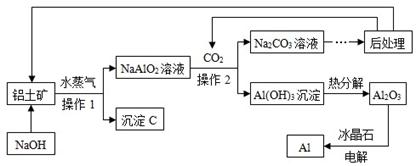
(1)工业生产中,要将铝土矿细磨预处理,目的是;
(2)沉淀C的化学式是;
(3)操作1、操作2的名称是,实验室完成此操作时,需要的玻璃仪器的是玻璃棒、烧杯和;
(4)此工艺中,可循环使用的物质是CO2、H2O和;(填化学式)
(5)电解Al2O3的化学方程式为;
(6)NaAlO2溶液中通入CO2反应的化学方程式是。
做完“铁在氧气中燃烧”实验后,小冬同学有两个疑惑不解的问题,于是她进行了以下探究活动,请你一同参与。
[问题1]铁燃烧时溅落下来的黑色物质中还有没有铁呢?
[查阅资料1]
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)铁的氧化物均能溶于酸溶液。
[实验探究]
将冷却后的黑色物质碾碎,装入试管,加入溶液,观察到的现象是,说明铁燃烧时溅落下来的黑色物质中还含有铁。
[问题2]铁燃烧的产物为什么不是Fe2O3呢?
[查阅资料2]
(1)Fe3O4和Fe2O3的分解温度、铁的熔点见右表: 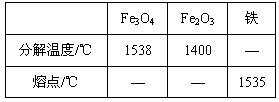
(2)Fe2O3高温时分解成Fe3O4。
[理论探讨]
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在之间,在此温度范围内Fe2O3已分解,所以铁在氧气里燃烧的产物是Fe3O4。
[拓展延伸]
(1)实验中为了防止集气瓶炸裂,必须;
(2)Fe2O3高温时会分解成Fe3O4和一种气体,请写出此反应的化学方程式;
(3)有些超市的食品密封包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色变为,就说明包装盒破损进气,这样售货员就能及时发现并处理。