实验室里用加热正丁醇、溴化钠和浓硫酸的混合物的方法来制备1—溴丁烷时,还会有溴、烯和醚等产物生成。反应结束后将反应混合物蒸馏,分离得到1—溴丁烷。已知有关物质的性质如下:
| |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
| 正丁醇 |
-89.53 |
117.25 |
0.81 |
| 1—溴丁烷 |
-112.4 |
101.6 |
1.28 |
| 丁醚 |
95.3 |
142 |
0.76 |
| 1—丁烯 |
-185.3 |
-6.5 |
0.59 |
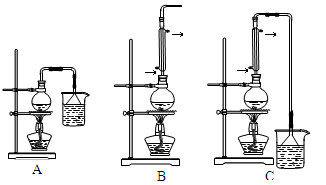
(1)生成1—溴丁烷的反应装置应选用上图中的 (填序号),反应加热时温度t1应控制在 100℃。
(2)生成1—溴丁烷的化学方程式为 。
(3)反应中由于发生副反应而生成副产物的反应类型依次有(按生成溴、烯、醚的先后顺序) 。
(4)反应结束后,将反应混合物中1—溴丁烷分离出,应采用方法是 ,该操作应控制温度t2的范围是 。
(5)在最后得到的1—溴丁烷的产物中,可能含有的杂质主要是 ,进一步除去的方法是 。
(6)在分液漏斗中用一种有机溶剂提取水溶液里的某物质时,静置分层后,欲知哪一层液体是“水层”,其简便的判断方法是 。
某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。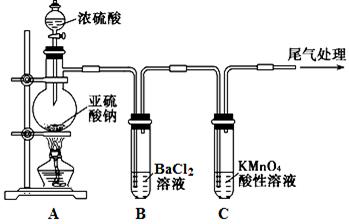
已知:Na2SO3+H2SO4(浓)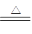 Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是。
(2)实验过程中,C中的现象是,说明SO2具有性。
(3)实验过程中,观察到装置B中出现了明显的白色沉淀。为探究该白色沉淀的成分,该小组同学进行了如下实验: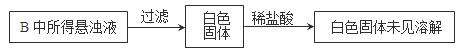
根据实验事实判断该白色沉淀的成分是(填化学式),产生该白色沉淀的原因可能是(填字母编号)。
a.BaSO3既不溶于水也不溶于酸
b.BaCl2溶液中可能溶解有氧气
c.BaCl2溶液中可能混有NaOH
d.由A制得的SO2气体中可能混有氧气
(4)如果将装置A中的浓H2SO4换作浓HNO3,对此实验是否有影响并明理由。
将氯气用导管通入较浓的NaOH和H2O2的混和液中,在导管口与混和液的接触处有闪烁的红光出现。这是因为通气后混和液中产生的ClO-被H2O2还原,发生激烈反应,产生能量较高的氧分子,然后立即转变为普通氧分子,多余的能量以红光放出。本实验所用的仪器及导管如图。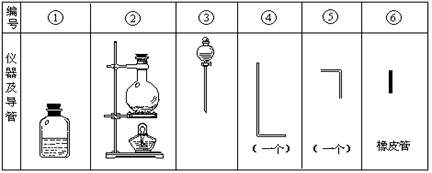
根据要求填写下列空白:
(1)组装氯气发生装置时,应选用的仪器及导管为 (填写图中编号)。
(2)本实验进行时,按气流方向从左到右的顺序,气体流经的各仪器及导管的编号依次为 。
(3)仪器①的橡皮塞上至少应有2个孔的原因是 。
(4)本实验需配置10mol·L-1的NaOH溶液500mL,用到的仪器除了托盘天平、烧杯外,还须用到的仪器有 (填仪器名称) ,定容时操作如图,则所配溶液浓度 (填“偏高”或“偏低”)。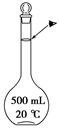
(5)实验时仪器①中ClO-与H2O2反应的离子方程式为 。
某化学兴趣小组的同学利用所示实验装置进行实验(图中a、b、c表示止水夹)。
请按要求填空:
(1)利用B装置可制取的气体有__________(填2种)。
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。若在丙中加入适量水,即可制得氯水。将所得氯水分成两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象结论如下:
请你评价实验Ⅱ结论是否合理?_____________;理由:______________。
(3)请利用上述A、C装置设计一个简单的实验,验证Cl2和Br2的氧化性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)_____________。
(4)B、D、E装置相连后,在B中盛装足量浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验。
①B中发生反应的化学方程式为____________________________。
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹a、b,再打开止水夹c,使烧杯中的水进入试管丁的操作是_______________________。
③试管丁中的NO2与一定量的O2混合充满后倒插水中,试管9/10充满水,则原试管丁中的混合气体平均相对分子质量可能为_________。(只填一种即可,保留二位小数)
浓硫酸有强氧化性,铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。请你协助他们探究所得气体的成分。
Ⅰ【提出猜想】
猜想1:所得气体中可能是SO2。 猜想2:所得气体中可能是__________。
猜想3:所得气体中可能是_______的混合气体。
Ⅱ【实验探究】
(1)将所得气体通入如下装置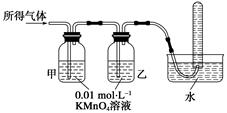
证明猜想3正确的实验现象是___________、______________、________________。
(2)点燃余下的气体前,必须要进行的操作是_________________________________。
(3)写出浓硫酸表现出强氧化性的化学反应方程式_____________________________。
(4)如果把一定量的铁与浓硫酸加热时产生的气体通过装有过量Na2O2粉末的玻璃管,则玻璃管中反应的生成物可能含有(填化学式)__________________ ___________ _。
铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
(1)试剂1是 ,加入新制氯水后溶液中发生的离子反应方程式是:,;
(2)加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是 ;
(3)在实验中发现放置一段时间,溶液的颜色会逐渐褪去。为了进一步探究溶液褪色的原因,甲、乙、丙三位同学首先进行了猜想:
| 编号 |
猜想 |
| 甲 |
溶液中的+3价Fe又被还原为+2价Fe |
| 乙 |
溶液中的SCN-被过量的氯水氧化 |
| 丙 |
新制的氯水具有漂白性,将该溶液漂白 |
基于乙同学的猜想,请设计实验方案,验证乙同学的猜想是否正确。写出有关的实验操作、预期现象和结论。(不一定填满,也可以补充)
| 编号 |
实验操作 |
预期现象和结论 |
| ① |
||