下列实验操作、现象和结论均正确的是
| 选项 |
实验操作 |
现象 |
结论 |
| A |
淀粉溶液中加稀硫酸,加热片刻,滴加银氨溶液,再水浴加热 |
无银镜生成 |
淀粉未发生水解 |
| B |
将一铝箔放在酒精灯外焰上灼烧 |
铝箔熔化但不滴落 |
铝箔表面生成致密的Al2O3薄膜,且Al2O3熔点高于Al |
| C |
铜放入稀硫酸中,再加入硝酸钠固体 |
开始无明显现象,后溶液变蓝,有明显的气泡放出,铜溶解 |
硝酸钠可以加快铜与稀硫酸的反应速率 |
| D |
向2 mL 0.1 mol/L Na2S溶液中滴几滴0.1 mol/L ZnSO4溶液;再加入几滴0.1 mol/L CuSO4溶液 |
先生成白色沉淀,后生成黑色沉淀 |
溶度积(Ksp):ZnS>CuS |
下图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于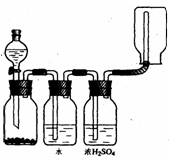
A锌和盐酸发生氢气
B二氧化锰和浓盐酸生成氯气
C碳酸钙和盐酸生成二氧化碳
D氯化钠和浓硫酸生成氯化氢
(1)已知:在1×105Pa条件下,氢气的标准燃烧热是285.8 kJ·mol-1,下列热化学方程式正确的是 ()
| A.H2O(g)=H2(g)+1/2O2(g)ΔH=+285.8kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l)ΔH=—517.6kJ·mol-1 |
| C.H2(g)+1/2 O2(g)=H2O(g)ΔH=—285.8kJ·mol-1- |
| D.2H2(g)+O2(g)=2H2O(l)ΔH=+517.6J·mol-1 |
(2)科学家盖斯曾提出:“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的。”利用盖斯定律可测某些特别反应的热效应。
① P4(s,白磷)+ 5O2(g)=P4O10(s);ΔH=—2983.2kJ·mol-1
② P(s,红磷)+ 5/4 O2 (g) ="1/4" P4O10(s)ΔH=—738.5kJ·mol-1-
则白磷转化为红磷的热化学方程式_________________________________。相同的状况下,能量较低的是_________;白磷的稳定性比红磷___________(填“高”或“低”)
在由Na2S、Na2SO3、Na2SO4组成的固体混合物中,已知S的质量分数为25.6% ,则氧的质量分数为:()
| A.36.8% | B.37.6% | C.51.2% | D.无法计算 |
某混合气体中可能含有H2、CO、CO2、HCl、NH3、和H2O(气)中的两种或多种,当混合气体依次通过:①澄清石灰水(无混浊现象);②氢氧化钡溶液(有混浊现象);③浓硫酸(无明显现象);④灼热的氧化铜(变红);⑤无水硫酸铜(变蓝)。对该混合气体成分的正确判断是( )
| A.一定没有CO2,肯定有H2 | B.一定有CO、CO2和H2O(气) |
| C.可能有CO2、NH3、和H2O(气) | D.一定有H2、CO2、HCl、 |
世界著名的科技史专家、英国剑桥大学的李约瑟博士考证说:“中国至少在距今3000年以前,就已经使用玻璃了。”下列有关玻璃的说法不正确的是()
| A.制普通玻璃的原料主要是纯碱、石灰石和石英 |
| B.玻璃在加热熔化时有固定的熔点 |
| C.普通玻璃的成分主要是硅酸钠、硅酸钙和二氧化硅 |
| D.盛放烧碱溶液的试剂瓶不能用玻璃塞,是为了防止烧碱跟二氧化硅生成硅酸钠而使瓶塞与瓶口粘在一起 |