某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯
已知:
| |
密度(g/cm3) |
熔点(℃) |
沸点(℃) |
溶解性 |
| 环己醇 |
0.96 |
25 |
61 |
能溶于水 |
| 环己烯 |
0.81 |
-103 |
83 |
难溶于水 |

(1)制备粗品:将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.
①A中碎瓷片的作用是 ,导管B除了导气外还具有的作用是 .
②试管C置于冰水浴中的目的是 .
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静置、分层,环己烯在______层(填上或下),分液后用______(填入编号)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图2所示装置蒸馏,冷却水从______口进入。蒸馏时要加入生石灰,目的是 .
③收集产品时,控制的温度应在____左右,实验制得的环己烯精品质量低于理论产量,可能的原因是____
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是______.
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点.
(10分)某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准硫酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入甲基橙作指示剂,进行滴定。滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗硫酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL蒸馏水,测得所耗硫酸为V2mL。
试回答下列问题:
(1)锥形瓶中的溶液从色变为 色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应注意观察
(3)上述操作步骤中两处错误分别是,
(请指出具体错误)。由此造成的测定结果分别是, (填偏高、偏低或无影响)。
(4)某次滴定时的滴定管中的液面如图,则其读数为mL。若记录读数时,起始时俯视,终点时仰视,则所测溶液浓度会(填偏高、偏低或无影响)。
(5)根据下列数据:
| 滴定次数 |
待测液体积(mL) |
标准硫酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
20.00 |
0.50 |
25.45 |
| 第二次 |
20.00 |
4.00 |
29.05 |
请计算待测烧碱溶液的浓度为mol/L。
某校化学小组的同学用如图装置对炭与浓硫酸的反应的产物进行验证,请回答以下问题:
(1)A中炭与浓硫酸反应的化学方程式;
(2)若要验证炭与浓硫酸反应的产物,用BCDE装置进行验证,所用药品如下
| A.品红溶液 | B.酸性高锰酸钾溶液 |
| C.澄清石灰水 | D.氢氧化钠溶液 |
其中B装置中的药品为,其作用是;
C装置中的药品,其作用是;
D装置中的药品,其作用是;
E装置中的药品,其作用是。
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。请回答:
(1)浓硫酸的作用是。
(2)球形干燥管C的作用是。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是;反应结束后D中的现象是。
下列有机实验操作或叙述中正确的是(填写代号)。
| A.制取酚醛树脂的实验中,水浴加热时不必用温度计 |
| B.苯和浓溴水反应可制溴苯 |
| C.验证蔗糖水解产物时,在蔗糖溶液中加几滴稀硫酸,水浴5min,加入新制银氨溶液 |
| D.向鸡蛋清溶液中滴入浓硝酸,会有白色沉淀产生,微热会产生黄色物质 |
E.在植物油中滴入溴水,溴水会褪色
F.实验室制肥皂时,将适量植物油、乙醇和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,即可得到肥皂
从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(一)海水淡化的方法主要有(填一种)
(二)从海水中提取溴和镁的流程如下图所示:
(1)提取Br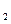 时第一次通入Cl
时第一次通入Cl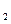 后发生反应的离子方程式是;②中表现
后发生反应的离子方程式是;②中表现 表现(填“氧化”或“还原”)性;
表现(填“氧化”或“还原”)性;
第二次通入Cl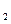 后,要提取Br
后,要提取Br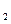 还要进行的操作为。
还要进行的操作为。
(2)为了实现对镁离子的富集,①中加入的足量试剂是(填化学式);
试从节约能源,提高金属镁的纯度分析,以下最适宜的冶炼的方法是(填字母)。