、现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| A |
有三个电子层,K、M层电子数之和等于L层电子数 |
| B |
短周期中金属性最强 |
| C |
常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D |
元素最高正价是+7价 |
(1)用化学用语回答下列问题:
B元素在周期表中的位置 ;
用电子式表示BD化合物的形成过程 。
(2)元素D与元素A相比,非金属性较强的是D,下列表述中无法证明这一事实的是 (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化(反应条件和个别生成物已略去)。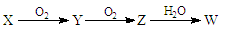
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,生成该白色沉淀的化学方程式为: ;
②若X是金属单质,则Z→W的反应中氧化剂与还原剂物质的量之比为 。
现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________mol。
(2)该气体所含原子总数为________个。
(3)该气体在标准状况下的体积为____________L。
(4)该气体溶 于1L水中(不考虑反应),其溶液中溶质的质量分数为_______。
于1L水中(不考虑反应),其溶液中溶质的质量分数为_______。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_____mol·L-1。
某校化学实验兴趣小组在“探究溴水与氯化亚铁溶液反应”的实验中发现:在足量的稀氯化亚铁溶液中,加入1—2滴溴水,振荡后溶液呈黄色。查阅资料显示:溴水是溴(Br2)的水溶液,呈黄色;溴水中含有溴单质。
⑴提出问题:Fe3+、Br2,谁的氧化性更强。
⑵猜想:
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含(填化学式,下同)所致
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含所致。
⑶设计 实验并验证
实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
除氯 化亚铁溶液和溴水外,还有供选用的试剂:
化亚铁溶液和溴水外,还有供选用的试剂:
a、酚酞试液;b、CCl4;c、无水酒精;d、KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到的现象(试剂填序号)
| 选用试剂 |
实验现象 |
|
| 方案1 |
||
| 方案2 |
⑷结论:氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入1— 2滴溴水,溶液呈黄色所发生的离子反应方程式为
2滴溴水,溶液呈黄色所发生的离子反应方程式为
⑸实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是(填离子的化学式)。
②在100mLFeBr2溶液中通入2.24LCl2(标准状况),溶液中有1/2的Br-被氧气成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为。
以海水中常见物质A为原料可以发展很多工业,下图中包含了中学课本中介绍的几种基本工业生产,请根据各物质之间的转化关系回答下列问题。
(1) C和D、C和G反应都可以制取消毒剂。C和D反应制取的消毒剂中有效成分的化学式为______ ____。
(2) 电解A溶液反应的离子方程式为________________________________。
(3) 将F和J通入A的饱和溶液中,反应的化学方程式为:
________________________________。
(4) J的空间构型为___________形。
(5)实验室可利用K与G制取J,请写出该反应化学方程式:______________________________________________________。
A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:
(1)常温下,若A为气态单质,c为非金属氧化物,A、C均能使品红溶液褪色,相对分子质量E>D,则该反应的反应方程式为:_____ ______
检验D中阴离子所用试剂为:
(2)若A为短周期的金属单质,D为气态单质,C溶液呈酸性或强碱性时,该反应都能进行。写出C溶液呈强碱性时反应的离子方程式:
(3)若A、C均为化合物,E为白色沉淀,C为引起温室效应的主要气体,写出E可能的物质的化学式(写两种):,。
水是生命之源,也是化学反应中的主角。试回答下列问题:
A.B.C是中学化学常见的三种有色物质(其组成的元素均属短周期元素),
它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,请写出
A.B.C与水反应的化学方程式:
(1) _____ _______
(2)
(3) 。