(5分)向100 mLBaCl2、AlCl3、FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀和加入混合溶液B的体积关系如下图所示:
(1)加入B溶液110 mL时,溶液中的沉淀是 ,溶液中的溶质是 。
(2)从90 mL至100mL之间加入10mL B溶液时发生的离子反应方程式是:
Ba2+ + SO42—→BaSO4↓,Al(OH)3 + OH— →AlO2— +2H2O
溶液B中Na2SO4与NaOH的物质的量浓度之比为 ;
(3)计算A溶液中AlCl3的物质的量浓度,写出计算过程:
(8分)将一定量的氧化铜加入到100.Og质量分数为19.6%的硫酸溶液中,完全溶解后溶液显蓝色,再加人19.6g铁粉充分反应后,经过滤、干燥得到的固体仍为19.6g。
(1)通过计算说明干燥后的固体是什么物质?
(2)求原氧化铜的质量。
将固体草酸锰MnC2O4·2H2O放在一个可以称出质量的容器中加热。固体质量随温度的变化关系如图所示。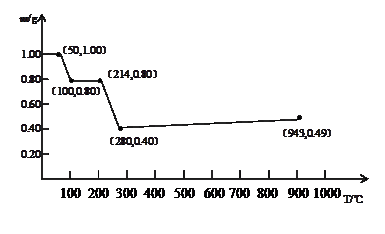
(1)214℃,剩余固体的成分为(填写化学式,下同);280℃时,剩余固体的成分为。
(2)当温度超过280℃时,剩余固体的质量又会增加,943℃完全生成另一种固体物质,则280℃-943℃过程中发生反应的化学方程式为。
(3)草酸锰受热可生成MnO2,MnO2是一种重要的无机功能材料,在硫酸锰溶液中加入NaClO可生成MnO2和Cl2,请写出向硫酸锰溶液中加入NaClO时发生反应的化学方程式。
现有碳酸氢钠和碳酸钠固体混合物,为了测定混合物中碳酸钠的百分含量,利用如下装置: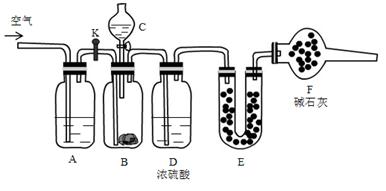
实验步骤:
①检查装置气密性
②将药品装好,其中B中装入 9.5g样品,E装好药品后,称量总质量56.0g
③关闭活塞K,打开分液漏斗活塞,放下液体,充分反应
④待B中完全反应后,打开活塞K,通入一会儿空气
⑤称量E装置质量为60.4 g
回答下列问题:
(1)C中装的药品是,E中药品是,F中药品的作用。
(2)A中发生反应的离子方程式为。
(3)样品中碳酸钠的质量百分含量为。
(4)若实验中后期不通入空气,则所测得样品中碳酸钠的百分含量(填“偏小”“偏大”“不影响”)
将1mol KClO3加强热至60%分解,将分解后得到的KCl和KClO3溶于过量稀硫酸并加热,试计算可以得到标况下氯气的体积?
小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打每片含0.50gNaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是mol
(2)胃舒平每片含0.245gAl(OH)3.中和胃酸时,6片小苏打相当于胃舒平片
(3)达喜的化学成分是铝和镁的碱式盐:
取该碱式盐3.01g,加入2.0mol/L盐酸使其溶解,当加入盐酸42.5mL时开始产生CO2,加入盐酸至45.0mL时正好完全反应,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比