一定温度下反应N2(g)+3H2(g)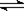 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
| A.单位时间里每增加1molN2,同时减少2molNH3 |
| B.c(N2)∶c(H2)∶c(NH3)=1∶3∶2 |
| C.N2与H2的物质的量与NH3的物质的量相等 |
| D.N2、H2和NH3的质量分数不再改变 |
体积相同的NaCl、MgCl2、AlCl3溶液,沉淀其中的Cl-,消耗等量的AgNO3,三种溶液的物质的量浓度之比为 ( )
| A.3∶2∶1 | B.1∶2∶3 | C.6∶3∶2 | D.2∶3∶6 |
NA为阿伏加德罗常数,对于1mol/L的硫酸溶液,下列叙述错误的是 ( )
| A.1000mL溶液中,含2NA个H+ |
| B.1000mL溶液中,含3NA个离子(H+、SO42-) |
| C.1000mL溶液中,加入足量Zn,可生成2NA个H2分子 |
| D.1000mL溶液中,加入足量Zn,可生成NA个Zn2+ |
1molSO2和1molSO3具有相同的①分子数②原子数③ S原子数④ O原子数 ( )
| A.①② | B.①③ | C.①④ | D.②④ |
下列叙述正确的是 ( )
| A.1摩尔氢为2克 | B.H2O的摩尔质量为18克 |
| C.44克CO2的体积为22.4L | D.9.8克H2SO4含0.1NA个H2SO4分子 |
天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴( ),充电时 中 被氧化, 迁移并以原子形式嵌入电池负极材料碳( )中,以 表示。电池反应为 ,下列说法正确的是
| A. | 充电时,电池的负极反应为 |
| B. | 放电时,电池的正极反应为 |
| C. | 羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质 |
| D. | 锂离子电池的比能量(单位质量释放的能量)低 |