有机物X(分子式为C4H6O5)广泛存在于许多水果中,尤以苹果、葡萄、西瓜、山楂内为多。经测定该有机物具有下表中所列性质,请根据题目要求填空:
(1)
| X的性质 |
推测X中关于官能团的结论 |
| ①X与足量Na反应产生H2 |
|
| ②X与醇或羧酸在浓硫酸作用下并加热均生成有香味的产物 |
|
| ③在一定条件下X的分子内脱水产物(非环状化合物)可与溴水发生加成反应 |
含—OH |
| ④33.5 g X与100 mL 5 mol·L-1 NaOH溶液恰好中和 |
|
(2)写出X发生①反应的化学方程式(任写一个) 。
(3)在一定条件下X可发生化学反应的类型有 。(填序号)
a.水解反应
b.取代反应
c.加成反应
d.消去反应
e.加聚反应
(4)下列物质与X互为同系物的是_______。与X互为同分异构体的是______ _(填序号)
400 mL NaNO3和AgNO3的混合溶液中c(NO3—)=4mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到11.2L气体(标准状况),假设电解后溶液体积仍为400 mL。回答下列问题:
(1)把下列电极方程式补充完整:
阴极:、2H++ 2e-= H2
阳极:
(2)上述电解过程中转移电子的物质的量为。
(3)电解后溶液中的c(H+)为
按下图装置进行实验,并回答下列问题
(1)判断装置的名称:A池为
(2)锌电极反应式为__________________
石墨棒C1为______极,电极反应式为__________
石墨棒C2附近发生的实验现象为______________
(3)当C2极析出2.24L气体(标准状态)时,锌的质量减少了__g.CuSO4溶液的质量增加了______g
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得,5g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式_________________。
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 |
H-H |
N-H |
N≡N |
| 键能/kJ·mol-1 |
436 |
391 |
945 |
已知反应N2+3H2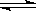 2NH3△H="a" kJ·mol-1。试根据表中所列键能数据估算a的数值为________。
2NH3△H="a" kJ·mol-1。试根据表中所列键能数据估算a的数值为________。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+02(g)=C02(g) △H1=-akJ·mol-1
2H2(g)+02(g)=2H20(l)△H2=-bkJ·mol-1
2C2H2(g)+502(g)=4C02(g)+2H20(l)△H3=-ckJ·mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变:△H=_________。
(4分)某温度时,2L容器中X、Y、Z三种物质的量随时间的变化如图所示。由图中数据分析,该反应的化学方程式为__;反应开始至2min ,Z的平均反应速率为。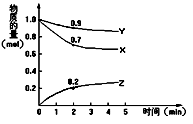
某微粒的结构示意图为 试回答:
试回答:
(1)当x-y=10时,该粒子为(填“原子”或“阳离子”“阴离子”)
(2)当y=8时,该粒子可能是(任写三种):、、。
(3)写出y=3的元素最高价氧化物与y=7的元素最高价氧化物对应水化物发生反应的
离子方程式。