在不同温度下,向VL密闭容器中加入0.5 mol NO和0.5 mol活性炭,发生反应:
2NO(g)+C(s)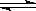 N2 (g)+CO2 (g) △H= —QkJ·mol-1 (Q>0),达到平衡时的数据如下:
N2 (g)+CO2 (g) △H= —QkJ·mol-1 (Q>0),达到平衡时的数据如下:
| 温度/℃ |
n (C)/mol |
n(CO2)/mol |
| T1 |
|
0. 15 |
| T2 |
0. 375 |
|
下列有关说法正确的是
A.由上述信息可推知:T1>T2
B.T2℃时,若反应达平衡后再缩小容器的体积,c(N2):c(NO)增大
C.T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率增大
D.T1℃时,该反应的平衡常数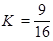
列各组物质的晶体中,化学键和晶体类型完全相同的是
| A.二氧化碳和二氧化硅 | B.氯化钠和氯化氢 |
| C.氢氧化钾和氯化钾 | D.二氧化硫和水 |
根据中学化学教材所附元素周期表判断,下列叙述不正确的是
| A.第15列元素的最高价氧化物的化学式为R2O5 |
| B.第2列元素中肯定没有非金属元素 |
| C.L层电子数为偶数的所有主族元素所在族的序数与元素原子L层电子数相等 |
| D.M层电子数为奇数的所有主族元素所在族的序数与元素原子M层电子数相等 |
银锌电池广泛用作各种电子仪器的电源,其电极分别为Ag2O、Zn,电解质溶液为KOH溶液,总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。下列说法中错误的是
| A.工作时,负极上发生反应的物质是Zn |
| B.溶液中OH-向正极移动,K+、H+向负极移动 |
| C.工作时,负极区溶液氢氧根浓度减小 |
| D.正极上发生的反应是Ag2O+H2O+2e-=2Ag+2OH- |
对于反应A+B=C+D,下列条件的改变一定使化学反应加快的是
| A.增加A的物质的量 | B.升高体系的温度 |
| C.减少C的物质的量 | D.增加体系的压强 |
下列反应中,生成物的总能量大于反应物的总能量的是
| A.氢气在氧气中燃烧 | B.焦炭在高温下与水蒸气反应 |
| C.铝与三氧化二铁高温反应 | D.铁丝在氧气中燃烧 |