(14分)苯乙烯(C6H5CH=CH2)是合成橡胶和塑料的单体,用来生产丁苯橡胶、聚苯乙烯等。工业上以乙苯(C6H5CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯,反应方程式为:
C6H5CH2CH3(g)  C6H5CH=CH2(g)+H2(g)
C6H5CH=CH2(g)+H2(g)  H
H
(1)已知:H2和CO的燃烧热( H)分别为-285.8 kJ.mol
H)分别为-285.8 kJ.mol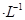 和-283.0 kJ.mol
和-283.0 kJ.mol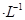 ;
;
C6H5CH2CH3(g)+CO2 (g) C6H5CH=CH2(g)+CO(g)+H2O(l)
C6H5CH=CH2(g)+CO(g)+H2O(l)  H=+114.8 kJ·mol-1
H=+114.8 kJ·mol-1
则制取苯乙烯反应的 H为_________
H为_________
(2)向密闭容器中加入1 mol乙苯,在恒温恒容条件下合成苯乙烯,达平衡时,反应的能量变化为QkJ。下列说法正确的是 _________。
| A.升高温度,正反应速率减小,逆反应速率增大 |
| B.若继续加入1 mol乙苯,苯乙烯转化率增大 |
| C.压缩体积,平衡逆向移动,反应物浓度增大,生成物浓度减小 |
| D.相同条件下若起始加入1 mol苯乙烯和1 mol氢气, |
达平衡时反应能量变化为( H-Q)kJ
H-Q)kJ
(3)向2 L密闭容器中加入1 mol乙苯发生反应,达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示。700 时,乙苯的平衡转化率为_______,此温度下该反应的平衡常数为 ______;温度高于970
时,乙苯的平衡转化率为_______,此温度下该反应的平衡常数为 ______;温度高于970 时,苯乙烯的产率不再增加,其原因可能是_________。
时,苯乙烯的产率不再增加,其原因可能是_________。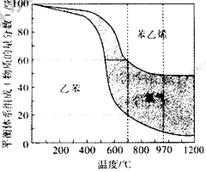
(4)含苯乙烯的废水排放会对环境造成严重污染,可采用电解法去除废水中的苯乙烯,基本原理是在阳极材料MOx上生成自由基MOx(OH),其进一步氧化有机物生成CO2,该阳极的电极反应式为_________,若去除0.5 mol苯乙烯,两极共收集气体_________mol。
灰锡结构松散,不能用于制造器皿,而白锡结构坚固,可以制造器皿,现把白锡制成的器皿放在0℃,100kPa的室内存放,它会不会变成灰锡而不能再继续使用?
已知:在0℃、100kPa条件下白锡转化为灰锡的反应焓变和熵变分别为△H=-2180.9J·mol-1,△S="-6.61" J·mol-1·K-1
摩尔熵是单位物质的量的物质在一定条件下所具有的熵。试比较下列两组物质摩尔熵的大小顺序。
(1)相同条件下的气态甲醇、乙醇、丙醇。
(2)气态苯、液态苯、固态苯。
已知在298.15K、100kPa下石灰石分解反应:
CaCO3(s)=CaO(s)+CO2(g)△H=+178.3kJ·mol-1△S=+160.4J·mol-1·K-1,试判断反应的自发性及自发进行的最低温度。
试判断用于汽车净化的一个反应2NO(g)+2CO(g)=N2(g)+2CO2(g)在298K、100kPa下能否自发进行?
已知:在298K、100kPa下该反应的△H=-113.0kJ·mol-1,
△S=-145.3 J·mol-1·K-1
(1)请描述金属晶体中自由电子的存在状态.
答:_____________________________________________________________.
(2)请说明金属晶体中自由电子所起的作用.
答:___________________________________________________________________.