氮化铝(AlN)是一种新型无机非金属材料。为了分析某AlN样品(样品中的杂质不与氢氧化钠溶液反应)中A1N的含量,某实验小组设计了如下两种实验方案。
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案l】取一定量的样品,用以下装置测定样品中AIN的纯度(夹持装置已略去)。
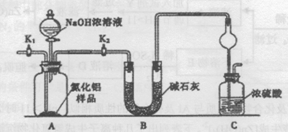
(1)上图C装置中球形干燥管的作用是 。
(2)完成以下实验步骤:组装好实验装置,首先 ,再加入实验药品。接下来的实验操作是 ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是 。
(3)若去掉装置B,则导致测定结果 (填“偏高”、“偏低”或“无影响”)。由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见 。
【方案2】按以下步骤测定样品中A1N的纯度:
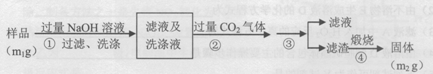
(4)步骤②生成沉淀的离子方程式为 。
(5)步骤③的操作是 。A1N的纯度是 (用m1、m2表示)。
实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验。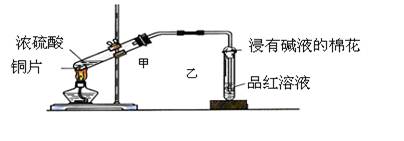
(1)根据什么现象可判断铜跟浓硫酸反应有SO2生成_____________________;
根据什么现象可判断铜跟浓硫酸反应有硫酸铜生成______________________;写出甲装置中发生的主要反应的化学方程式。
(2)装置乙的试管口部放有一团浸有碱液的棉花,棉花中通常是浸有饱和碳酸钠溶液,其作用是_________。
(3)实验完毕后,取少量乙试管中溶液于试管中加热,现象是;原因是。
某研究性学习小组的课题为“Mg—Cu硫酸原电池电解CuCl2溶液的研究”,他们的研究装置如下图所示(C1、C2均为碳棒),按要求填写下列空格。
(1)铜片上的现象是,该极的电极反应式为。
(2)C1极的名称为,C2极的电极反应式为。
(3)下列关于该装置中电子流向的叙述中正确的是。
| A.从镁电极经导线流向C1极 | B.从C1极经导线流向镁电极 |
| C.从铜电极经导线流向C2极 | D.从C2极经导线流向铜电极 |
(4)原电池中稀硫酸的体积为200 mL ,物质的量浓度为1.5 mol·L-1,当电解池中某碳棒上产生3.36 L(标准状况)气体时,求:
①有 个电子通过了电线(NA=6.02×1023)。
②此时原电池溶液中H+的物质的量浓度为 mol/L(不考虑溶液体积变化)。
按图所示实验过程填空:
(1)写出上述反应的离子方程式:
①②③
(2)填空:
ab cd
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。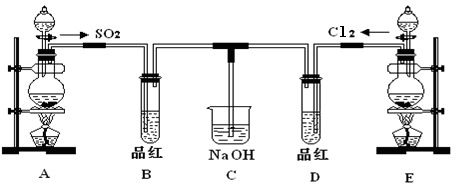
(1)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B:________________________________,D:____________________________。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为
B:________________________________,D:____________________________。
(2)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象那样。请你分析该现象的原因(用化学方程式表示)________________
(3)实验结束后,有同学认为装置C中会含有Na2SO4,如何验证Na2SO4是否存在?
亚硝酸钠是一种工业盐,现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
已知:①NO+NO2+2OH-=2NO2-+H2O
②气体液化的温度:NO2 21℃、NO -152℃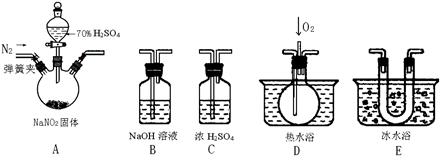
(1)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接):
A 、C、、、。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是:
。
(3)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是。
②装置E的作用是。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为。如果没有装置C,对实验结论造成的影响是。
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是。