如何将粗盐中的难溶性杂质(主要是泥沙)和可溶性杂质(主要是氯化镁、氯化钙)除去,从而得到较为纯净的食盐晶体?
【实验方案】某同学为了提纯粗盐,设计了以上实验方案并进行实验
【交流与表达】
(1)实验操作X的名称是 ,该操作中要用到的玻璃仪器有烧杯、玻璃棒和 ;
(2)实验步骤③的主要目的是 (用化学方程式回答);判断氢氧化钠溶液已过量的方法是 ;
(3)实验④中生成的沉淀D是 (填化学式);
【反思与评价】
(4)有同学认为原实验方案不完善,做出这种评价的依据是 ;
【实验方案再设计】
(5)为了完善原实验方案,你设计的实验是 (仅写出补充部分的实验操作和现象)
化学小组同学在加热二氧化锰样品时,发现有气泡产生(如图一所示),于是他们对这个异常现象进行了探究。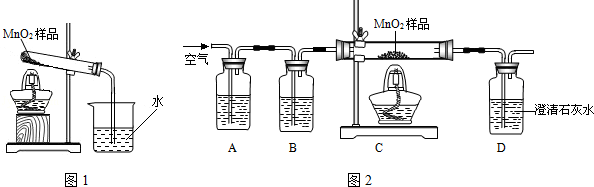
(1)对气体成分的探究:加热二氧化锰样品,用燃着的木条靠近试管口,木条熄灭。将气体通入澄清的石灰水,发现石灰水变浑浊,产生的气体是。
(2)对气体来源的探究:
甲同学认为:该气体来自于试管中的空气,请你设计实验证明该假设不成立
| 实验步骤及现象 |
结论 |
| 加热空的试管,另一端的澄清石灰水没有变浑浊 |
假设(填“不成立”或“成立”) |
乙同学认为:二氧化锰样品中可能混有炭粉,炭粉发生反应生成了该气体。他设计了如图二所示的实验进行研究,其中B装置的作用是检验A中反应是否完全,B中的试剂是,实验中观察到D处澄清石灰水变浑浊。他又用氮气代替空气(氮气不参与该实验中的任何反应),重复上述实验,发现D处澄清的石灰水也变浑浊。通过乙同学的实验证明,二氧化锰中混有炭粉,炭粉与反应产生了这种气体。
为了提高实验探究能力,老师为同学们提供了一包白色粉末,它可能是碳酸钙、氢氧化钙或两种物质的混合物。
(1)同学们设计了以下三种实验方案:
方案Ⅰ:取样品加入试管中,滴加稀盐酸,有气泡产生则白色粉末是碳酸钙。
方案Ⅱ:取样品加入试管中,滴加稀盐酸,无气泡产生则白色粉末是氢氧化钙。
方案Ⅲ:取样品加入试管中,加水振荡,静置,下层有不溶物,上层清液中滴入酚酞溶液,溶液变红,则白色粉末是碳酸钙和氢氧化钙的混合物。
以上三种方案中,你认为不合理的是(填方案序号),其不合理的理由是。
(2)请再设计一种方案,证明该粉末是两种物质的混合物,简要写出实验的操作、现象及结论。
| 操作步骤 |
实验现象及结论 |
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。小蔡很感兴趣,于是,他和同学们进行探究。
提出问题:过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
猜想:①可能有一种气体和另一种物质生成
②反应过程中可能有热量放出
设计装置如图所示
实验探究:实验一:探究反应后生成的气体是什么?
(1)打开上图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是。
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:。
实验二:继续探究反应后生成的另一种物质是什么?
(1)小张猜想另一种物质是Na2CO3,小蔡认为不可能.小蔡的依据是:。
(2)小蔡取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈性。
表达:由实验探究的结果,写出过氧化钠和水反应的化学方程式。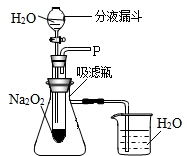
某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品,反应的化学方程式为:
2NaCl+2H2O 2NaOH+H2↑+Cl2↑。某研究性学习兴趣小组对该厂生产的烧碱样品进行如下探究。
2NaOH+H2↑+Cl2↑。某研究性学习兴趣小组对该厂生产的烧碱样品进行如下探究。
[提出问题]:烧碱样品中含有哪些杂质?
[猜想]:
(1)可能含有NaCl,作出此猜想的依据是电解的过程中氯化钠没有完全反应。
(2)可能含有碳酸钠,做出此猜想的理由是(用化学方程式表示)。
[实验设计]
| 实验步骤 |
实验现象 |
解释或结论 |
| ①取适量的烧碱样品置于试管中加水溶解,用手触摸试管外壁。 |
试管外壁发热。 |
原因是 |
| ②向①所得的溶液中加入盐酸至过量。 |
开始时无明显现象,过一段时间后有气泡产生。 |
说明样品中含有杂质 |
| ③向②所得的溶液中加入硝酸银溶液。 |
有白色沉淀产生。 |
AgNO3+NaCl=AgCl↓+NaNO3 说明样品中含有杂质氯化钠 |
[反思]:小明认为上述实验不能说明样品中含有氯化钠,理由是。
天然气的主要成分是甲烷(CH4),我校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】
甲 CO2 、H2O ;乙 CO、H2O;
丙 NH3、CO2 、H2O;丁 CO2 、CO、H2O 。
你认为同学的猜想是错误的,理由是。
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置: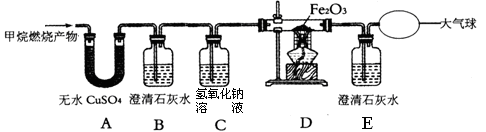
(1)若实验中观察到A中无水CuSO4变蓝,B、E中澄清石灰水变浑浊,D中红色粉末变成黑色,由此推断同学猜想成立,请写出甲烷在此时燃烧的化学方程式。
(2)A、B装置的顺序不能颠倒,其理由是,C装置的作用是;
【反思与交流】为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是。