在一定条件下,Na2CO3溶液存在水解平衡: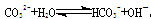 。下列说法正确的是
。下列说法正确的是
| A.稀释溶液,水解平衡常数增大 |
| B.通入CO2,平衡朝正反应方向移动 |
C.升高温度,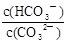 减小 减小 |
| D.加入NaOH固体,溶液pH减小 |
Na2FeO4是一种高效多功能水处理剂,一种制备Na2FeO4的方法可用化学方程式表示为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应说法不正确的是
| A.Na2O2在反应中既作氧化剂又作还原剂 |
| B.O2是氧化产物 |
| C.Na2FeO4既是氧化产物又是还原产物 |
| D.2 mol FeSO4发生反应时,共有12 mol电子转移 |
常温下,在溶液中可发生以下反应:
①16H++10Z-+2XO4-===2X2++5Z2+8H2O;
②2M2++R2===2M3++2R-;
③2R-+Z2===R2+2Z-。
由此判断下列说法错误的是
| A.常温下可发生反应2M2++Z2===2M3++2Z- |
| B.还原性强弱顺序为:X2+<Z-<R-<M2+ |
| C.Z元素在反应①中被氧化,在③中被还原 |
| D.氧化性强弱顺序为:XO4-<Z2<R2<M3+ |
某温度下,V mL不饱和NaNO3溶液a g,蒸发掉b g水或加入b g NaNO3固体(恢复到原温度)均可使溶液达到饱和,则下列量的计算结果正确的是
| A.该温度下NaNO3的溶解度为200 g |
B.原不饱和溶液中NaNO3的质量分数为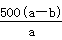 % % |
C.原不饱和溶液中NaNO3的物质的量浓度为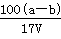 mol/L mol/L |
D.原不饱和溶液的密度为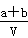 g/mL g/mL |
在相同的温度和压强下,4个容器中分别装有4种气体。已知各容器中的气体和容器的容积分别是a.CO2,100 mL;b.O2,200 mL;c.N2,400 mL;d.CH4,600 mL,则4个容器中气体的质量由大到小的顺序是
| A.a>b>c>d | B.b>a>d>c |
| C.c>d>b>a | D.d>c>a>b |
下列物质的分离方法中,是利用密度不同达到分离的是
| A.把石油经蒸馏分离成为汽油,煤油和柴油等 |
| B.煎中药时用水在煮沸条件下提取中药的有效成分 |
| C.把大豆磨碎后,用水溶解其中的可溶性成分,经过滤后,分成豆浆和豆渣 |
| D.做饭洗米时淘去米中的沙 |