下图是实验室制取某些常见气体所使用的一些装置和仪器。
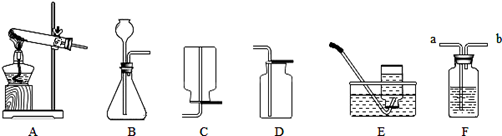
(1)写出实验室制取氧气的一个反应原理 ,用该方法制取氧气的发生和收集装置可选择 。
(2)实验室制取二氧化碳,应选择的发生和收集装置是 。欲收集满一瓶二氧化碳气体,需要用燃着的小木条放在集气瓶口,若观察到火焰熄灭,则接下来应进行的操作是 。若火焰不熄灭,则说明二氧化碳还没有收集满,应该继续收集。
(3)F装置的用途很广,下列关于该装置的用法正确的是 。
(将正确答案的序号填在横线上)
| A.当装置内盛满水,若收集氢气,气体从b通入,若收集氧气,气体从a通入。 |
| B.当装置内盛有一半的浓硫酸时,除去氢气中的水蒸气,气体从b通入 |
| C.当装置内盛满氧气时,将装置内的氧气排除来,水从a通入 |
| D.当装置内盛有一半的水时,观察给病人输氧气的速率,a端连接氧气钢瓶,b端连接病人。 |
将V1mL3.65% HCl溶液逐滴滴入盛有V2mL未知浓度的
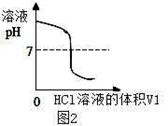
NaOH溶液的烧杯中(图1),测量并记录溶液的pH变化(图2)和
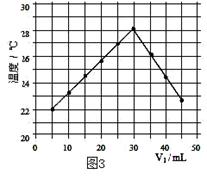
温度变化(图3)。(实验中始终保持 V1+V2=50.0mL且各种溶液密度
均为1.0g/mL)。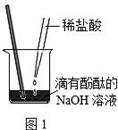
(1)图2中V1="0" mL时,图1中烧杯内溶液的颜色显色;
(2)实验中发生反应的化学方程式为;
(3)图2中的pH=7时,此时滴入的HCl溶液的体积V1=mL;
(4)通过该实验给出的判断,其中正确的是;
| A.进行该实验时环境温度为22℃ |
| B.该实验表明化学能可转化为热能 |
| C.该实验表明有水生成的反应都是放热反应 |
| D.溶液由碱性转变为中性,再转变为酸性且酸性不断减弱 |
(5)实验中所用NaOH溶液的溶质质量分数为。
硝酸钾是初中化学常见的一种物质。请按要求填空:
(1)质量分数为4.04%的硝酸钾(KNO3)溶液可作为无土栽培的营养液。该营养液(填“属于”或“不属于”)复合肥;
(2)在硝酸钾溶液中,共有三种微粒,它们是K+、NO3-和(用符号表示);
(3)黑火药爆炸的反应原理是:2KNO3+S+3C K2S+3CO2↑+N2↑,此反应的反应物和生成物中,没有涉及到下列物质类别中的(填序号)
K2S+3CO2↑+N2↑,此反应的反应物和生成物中,没有涉及到下列物质类别中的(填序号)
| A.单质 | B.氧化物 | C.酸 | D.碱 E.盐 |
(4)如右图,硝酸钾的溶解度随温度的升高而,50℃时,硝酸钾和氯化钠饱和溶液降温至20℃后,硝酸钾的溶质质量分数氯化钠的溶质质量分数(填“﹥”、“﹦”或“﹤”),欲将接近饱和的 KNO3溶液变成饱和溶液,可采取的方法有(列举一种)。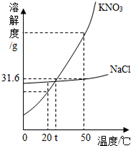
金属材料在工业上有广泛的用途。
(1)铝合金材质与纯铝比较,主要优点是;
(2)钢铁的锈蚀主要是铁与空气中的共同作用的结果,工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为;
(3)为了避免钢铁腐蚀,通常在钢铁外壳上镶嵌比铁活动性强的金属。小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图的两个实验: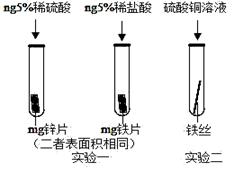
①实验一,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是;②实验二,若出现现象,可证明铁的活动性强于铜,该反应的化学方程式为。
化学是以实验为基础的科学。根据所学知识,完成下列问题。
(1)实验A中标号为①的仪器名称是,实验A制取氧气发生的化学方程式为;
(2)实验B的操作是违规的,正确方法是;
(3)实验C中烧杯③的作用是;
(4)实验D中,气球的变化情况是先变大后变小,写出导致气球变小的化学方程式。
请根据要求填空:
(1)汽车尾气装置发生的反应是:2NO+2CO→N2+2CO2,该反应的基本类型是;
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 E.不属于上述中的一种 |
(2)DNA水解产物中的胸腺嘧啶(C3H6N2O2),该物质中氮元素与氧元素的质量比为;
(3)可燃冰的主要成分是甲烷(CH4),写出其燃烧的化学反应方程式。