化学是一门以实验为基础的自然科学。依据实验目的设计切实可行的实验方案,是科学探究中的重要环节。
(1)用甲装置测定水的组成。正极与负极产生气体的质量比为_________。甲装置中发生反应的化学方程式为________________________。
(2)小红同学用乙装置进行探究实验,观察现象得出结论。
①“蜡烛中含有氢元素”,该判断所依据的现象是 。
②一段时间后,小红观察到蜡烛熄灭,由此得出可燃物燃烧必须具备的条件之一是 。
(3)用丙装置测定空气中氧气的含量。下列有关该实验的说法中,错误的是 (填字母序号)。
| A.实验时红磷一定要足量 |
| B.点燃红磷前先用弹簧夹夹紧乳胶管 |
| C.红磷熄灭后立刻打开弹簧夹 |
| D.最终进入瓶中水的体积约为消耗氧气的体积 |
现有八种物质,选择相应物质的字母填空:
A纯碱 B武德合金 C硝酸钾 D过磷酸钙
E.石墨 F.熟石灰 G.生石灰 H.干冰
(1)可用作复合肥料; (2)可用作食品干燥剂;
(3)可制作保险丝;(4)可用作电极。
(5)可用作配制波尔多液; (6)可作制冷剂。
以下是我们日常生活中常用各种清洗剂。
| 名称 |
洗涤灵 |
洁厕灵 |
炉具清洁剂 |
活氧彩漂 |
污渍爆炸盐 |
| 产品样式 |
 |
 |
 |
 |
 |
| 有效成分 或功能 |
清洗油污 |
盐酸 |
氢氧化钠 |
过氧化氢 |
过碳酸钠 |
(1)我们使用洗涤灵清洗餐具上的油污,这是因为它具有的功能。
(2)清除以下物质,可以使用洁厕灵的是填字母序号)。
A.铁锈 B.水垢(主要成分为碳酸钙和氢氧化镁)
C.油渍 D.氢气还原氧化铜实验后,试管内壁残留的红色固体
(3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2。将爆炸盐溶于水后,再加入足量的洁厕灵,产生能使澄清石灰水变浑浊的气体,这一反应了体现右图中(选填①②③④)性质关系。
(4)将洁厕灵滴入炉具清洁剂中,如图甲所示。
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外) ;此时溶液可用图乙中点处(选填A、B、C)表示。
②若反应后溶液pH为7,图丙中a微粒的化学式为。
(5)①“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(—O—O—)。据此推测,下列物质中,可用作杀菌消毒剂的是(填序号)。
②氧化氢溶液常用于医用消毒,某兴趣小组为测定一瓶久置的医用过氧化氢溶液中溶质质量分数。他们取该溶液51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示。试计算该过氧化氢溶液中溶质的质量分数。
(写出计算过程)
金属在生产生活中应用广泛。
(1)下图是铝的原子结构示意图。下列说法不正确的是。
A.铝原子的质子数为13 B.化合物中铝元素通常显+3价
C.铝是地壳中含量最多的元素 D.铝可作导线是由于它具有良好的导电性
(2)21世纪是钛的世纪。下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程: 
①反应Ⅰ在800~900 ℃的条件下进行,还生成一种可燃性无色气体,该反应的化学方程式为___ __;
②反应II可获得海锦钛,化学方程式表示为TiCl2+2Mg高温Ti+2MgCl2。该反应属于
(填序号)。
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
③该工艺流程中,可循环利用的两种物质是、。
(3)现有铝、铁、铜、银四种金属相互转化关系如图所示。 试推理乙是;写出甲→丙反应的化学方程式。
(4)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是 。
A.a点溶液中的溶质有4种
B.c点溶液中溶质为Zn(NO3)2
C.若取b~c段溶液,滴加稀盐酸,有白色沉淀
D.取d点的固体,加入稀盐酸,有气泡产生
(5)相同质量的锌、铁分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸)关系如下图所示,其中正确的是。
水是生命之源,是自然界中重要的物质。
(1)下图装置可以探究水的组成。通电一段时间后,试管1中所收集的气体为。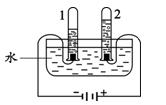
(2)下图是某品牌净水器中的过滤芯,里面装有精细滤网、活性炭、离子交换树脂、超细滤膜。离子交换树脂可减少水垢的形成,精细滤网和超细滤膜主要起作用,活性炭主要起作用。
(3)若某粗盐中只含泥沙、MgCl2两种杂质,校化学兴趣小组取ag该粗盐固体进行以下提纯探究。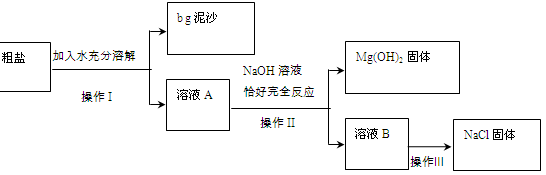
操作I、II中玻璃仪器有烧杯,玻璃棒,。
溶液A中的溶质是(写化学式)。
③ 溶液A与NaOH溶液反应生成Mg(OH)2固体的化学方程式为。
④ 最后得到的NaCl固体的质量____(a-b)g。(选填“<、>、=”)
以下是实验室常用的气体制备、收集的装置。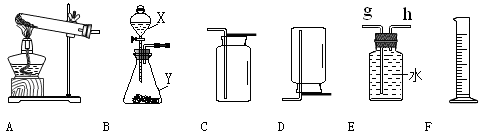
(1)若实验室用A装置制取氧气,其化学方程式为。
(2)若用C装置来收集CO2气体,则检验CO2已收满的方法是。
(3)若实验室用锌粒和稀硫酸制取氢气,反应的化学方程式为 ,可选择的发生装置是。若用E、F装置进行组合来收集并测定氢气的体积,则氢气应从E装置的(填“g”或“h”)导管口进,仪器F的名称是。
(4)对锌与稀硫酸反应快慢的影响因素进行探究。反应过程中,利用前10min 内收集的氢气体积比较反应的快慢。控制其他条件相同,进行下表四组实验,获得数据如下:
| 实验编号 |
试剂 |
前 10 min 内产生的氢气体积(mL) |
|
| 不同纯度的锌 |
不同体积和溶质质量分数的稀硫酸 |
||
| a |
纯锌 |
30mL 30% |
564.3 |
| b |
含杂质的锌 |
30mL 30% |
634.7 |
| c |
纯锌 |
30mL 20% |
449.3 |
| d |
纯锌 |
40mL 30% |
602.8 |
①比较实验a和实验b,可以得到的结论是。
②要比较不同溶质质量分数的硫酸对反应快慢的影响,应选择的是(填实验编号)。