(16分)甲、乙、丙三位同学在实验室用不同方法制取氮气。
(1)甲同学让空气通过右图所示装置,以除去氧气制得氮气。硬质玻璃管中所盛固体可选用 (填下列选项标号)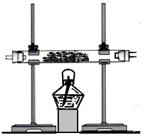
A.铁粉 B.碳粉 C.过氧化钠 D.碱石灰
(2)收集氮气可选用 (填下列选项标号)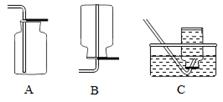
(3)乙同学设计用氨气和炽热的氧化铜反应制取氮气,反应方程式为 。
(4)制取氨气可选用 (填下列选项标号)
A.加热硫酸铵与氢氧化钙混合物
B.加热分解氯化铵晶体
C.浓氨水滴入氢氧化钠固体
D.加热浓氨水使氨气化
(5)丙同学用加热两种含氮溶液制氮气:NaNO2+NH4Cl  NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
该实验装置需要 、分液漏斗、酒精灯等玻璃仪器。
(6)氮气助燃金属镁,反应方程式 ;燃烧3.6 g镁将消耗标准状况下氮气 mL.
利用某炉渣 (只含Fe2O3、FeO、SiO2、Al2O3)可制备新型净水剂碱式氯化铝[Al2(OH)nCl6-n] 和Fe2O3。工艺流程如下:
(只含Fe2O3、FeO、SiO2、Al2O3)可制备新型净水剂碱式氯化铝[Al2(OH)nCl6-n] 和Fe2O3。工艺流程如下:
①用3.00mol/L的盐酸稀盐酸浸取炉渣,过滤.
②滤液先用H2O2氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3
③将第②步分离出沉淀的滤液通CO2调pH值后,保持温度在90~100℃进行“蒸发浓缩”,可以得到碱式氯化铝[Al2(OH)nCl6-n]
据以上信息回答下列问题:
(1)实验室配制3.00mol/L的盐酸100mL需要36.5%的浓盐酸(密度为1.2g/cm3) _____mL,配制用到的仪器有烧杯、玻璃棒、量筒、胶头滴管、。
(2)写出H2O2与滤液反应的化学方程式
(3) “蒸发浓缩”需保持温度在90~100℃,可采用的加热方法是
(4)为验证炉渣中含有Fe2O3,做如下实验:
a取适量炉渣于烧杯中,加足量溶解、静置
b取上层清液少量于试管中,滴加,观察现象。选用提供的试剂,
提供的试剂:①稀硝酸 ②稀硫酸 ③氯水 ④KMnO4溶液 ⑤ KSCN溶液
步骤a、b中所加试剂分别为;
步骤b中反应的离子方程式:
(16分)实验室需要0.1 mol·L-1NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是____________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。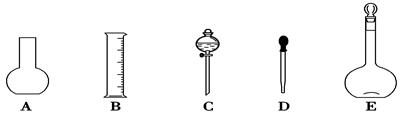
(2)下列是通过使用质量分数为98%(密度为1.84 g·cm-3)的浓硫酸来配制500 mL 0.5 mol·L-1硫酸溶液的操作步骤,其正确的操作顺序是(填序号)。
A.把容量瓶活塞塞上,反复摇匀后,装贴标签以保存
B.加入蒸馏水进容量瓶中进行定容,待水面离刻度线只有1~2厘米时,采用胶头滴管滴加蒸馏水使其凹液面正好与刻度线相切
C.在烧杯中注入适量的蒸馏水,用量筒准确量取98%的浓硫酸13.3ml慢慢注入烧杯中,并不停地搅拌使之稀释均匀
D.通过计算需要量取98%(密度为1.84 g·cm-3)的浓硫酸13.3ml
E.待烧杯中稀释的硫酸溶液冷却至室温后,通过玻璃棒引流转移至500ml的容量瓶中
F.把玻璃棒和烧杯分别都洗涤2~3 次,洗涤液也转移至容量瓶
次,洗涤液也转移至容量瓶
(3)根据计算用 托盘天平称取NaOH的质量为________g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol·L-1(填“大于”“等于”或“小于”,下同);若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________0.1 mol·L-1;溶解NaOH后在未降至室温时,立即将N
托盘天平称取NaOH的质量为________g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol·L-1(填“大于”“等于”或“小于”,下同);若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________0.1 mol·L-1;溶解NaOH后在未降至室温时,立即将N aOH溶液转移至容量瓶定容,则所得溶液浓度_______ 0.1 mol·L-1。
aOH溶液转移至容量瓶定容,则所得溶液浓度_______ 0.1 mol·L-1。
(4)在容量瓶的使用方法中,下列操作不正确的是(填写标号).
A.使用容量瓶前检查它是否漏水.
B.容量瓶用蒸馏水洗净后,不需要进行烘干就可以直接使用.
C.配制溶液时,如果 试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用滴管滴加蒸馏水到标线.
试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用滴管滴加蒸馏水到标线.
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用滴管滴加蒸馏水到标线.
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视。直到溶液由黄色变为橙色,并为止。
(2)下列操作中可能使所测NaO H溶液的浓度数值偏低的是。
H溶液的浓度数值偏低的是。
| A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束后俯视读数 |
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为mL,终点读数为mL;所用盐酸溶液的体积为 mL。
mL。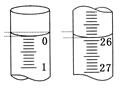
草酸晶体的组成可表示为H 2C2O4·xH2O,为测定x值,进行下列实验:①称取Wg草酸晶体配成100.0 mL水溶液;②取25.0 mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol·L-1的KMnO4溶液滴定,滴定时,所发生的反应为:
试回答下列问题:
(1)配平上述化学方程式。
(2)该实验滴定时,指示剂应该 (填“加”或“不加”)。
(3)若滴定时,反应前后的两次读数分别为a mL和b mL,则实验测得的所配草酸溶液的物质的量浓度为 ;由此计算出草酸晶体的x值是 。
(4)若滴定时所用KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 (填“偏大”、“偏小”或“无误差”)
(5)在滴定过程中,常常将锥形瓶的内壁用清水冲洗一下,原因是: 。
酸碱中和滴定是中学化学常见实验。
某同学欲测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
| A.冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。 |
| B.量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。 |
C.将酸式滴定管和碱式滴定管 用蒸馏水洗涤干净,并用各待盛溶液润洗。 用蒸馏水洗涤干净,并用各待盛溶液润洗。 |
| D.将物质的量浓度为1.50mol·L-1标准NaOH溶液装入碱式滴定管,调节液面记下读数V1。 |
E.继续滴定至终点,记下读数为V2。
F.在锥形瓶下垫一张白纸,把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G.量取浓硫酸样品5mL,在烧杯中用蒸馏水溶解。
H.重复以上实验。
请回答下列问题:
(1)操作步骤的顺序为 → A→ → →D→ → → H(用字母填写)。
(2)量取5mL浓硫酸的仪器是 ;量取20.00mL稀硫酸的仪器是 。
(3)选用的指示剂是 。
(4)判断到达滴定终点的现象是 。
(5)下表是实验测得的有关数据:
| 滴定 序号 |
待测稀硫酸 的体积(mL) |
所消耗NaOH标准溶液液的体积(mL) |
|
| V1 |
V2 |
||
| ① |
20.00 |
0.50 |
22.60 |
| ② |
20.00 |
6.00 |
27.90 |
请计算出该浓硫酸样品的浓度为 mol·L-1(不必写出计算过程)。