设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0.1NA |
| B.10g46%的乙醇水溶液中所含氢原子数目为1.2NA |
| C.高温下,0.2mol的铁与足量的水蒸气反应,生成氢气的分子数目为0.3NA |
| D.25℃时,100mlpH=13的Ba(OH)2溶液中OH-的数目为0.02NA |
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是
| 氧化物 |
环境问题 |
主要来源 |
|
| A |
CO2 |
酸雨 |
化石燃料的燃烧 |
| B |
SO2 |
光化学烟雾 |
汽车尾气的排放 |
| C |
NO2 |
温室效应 |
工厂废气的排放 |
| D |
CO |
CO中毒 |
燃料的不完全燃烧 |
将4 molA气体和2 molB气体在2 L的容器中混合并在一定条件下发生如下反应2A(g)+B(g) 2C(g),若经2 s后测得C的浓度为0.6 mol/L,现有下列几种说法:
2C(g),若经2 s后测得C的浓度为0.6 mol/L,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol/(L·s)
②用物质B表示的反应的平均速率为0.6 mol/(L·s)
③2 s时物质A的浓度为为1 mol/L
④2 s时物质B的浓度为0.7 mol/L
其中正确的是
| A.①③ | B.①④ | C.②③ | D.③④ |
等质量的两份锌粉a、b中分别加入过量的稀硫酸,同时向a中加入少量的CuSO4溶液,下列各图表示的是产生H2的体积V与时间t的关系,其中正确的是()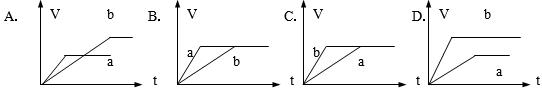
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是()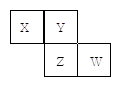
| A.原子半径:W> Z>Y>X |
| B.最高价氧化物对应水化物的酸性:Z>W>X |
| C.4种元素的单质中,Z单质的熔、沸点最低 |
| D.W单质能与水反应,生成一种具有漂白性的物质 |
如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c、d为两个电极。则下列有关的判断不正确的是()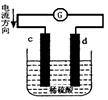
| A.d为负极,发生氧化反应 |
| B.c为锌片,电池工作时,溶液中SO42-向c移动 |
| C.电池工作的过程中,d电极上产生大量的气泡 |
| D.电池工作的过程中,溶液中SO42-浓度基本不变 |