往1.0 mol·L-1KI溶液中加入固体I2,发生反应:I2(aq)+I-(aq) I3-(aq) △H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示。已知反应第一次达到平衡时用时10s,则下列说法正确的是
I3-(aq) △H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示。已知反应第一次达到平衡时用时10s,则下列说法正确的是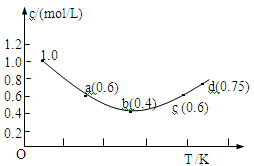
| A.该反应的△H>0 |
| B.a、c两点对应的I-反应速率相等 |
| C.b点时0~10s I-的平均反应速率为0.04mol·L-1·s-1 |
| D.d点时该反应在对应温度下处于平衡状态 |
关于硝酸的性质,下列说法不正确的是
| A.稀硝酸与Zn反应生成H2 | B.浓硝酸与C反应生成CO2 |
| C.Cu与稀硝酸、浓硝酸都能发生反应 | D.常温下,Fe在浓硝酸中发生钝化 |
下列气体不能用浓硫酸干燥的是
| A.Cl2 | B.NO2 | C.NH3 | D.SO2 |
常温下某集气瓶中气体呈红棕色,加入适量水后,盖上瓶盖振荡,得到无色溶液,气体的红棕色消失,再打开瓶盖后,瓶中又呈红棕色,则原瓶中气体可能是
| A.NO2 | B.Br2 | C.NO | D.N2 |
在开发利用金属矿物和海水资源过程中,下列说法不正确的是
| A.工业上可用电解法冶炼得到金属铝 |
| B.海水蒸发制海盐的过程中只发生了化学变化 |
| C.海水淡化的方法主要有蒸馏法、离子交换法等 |
| D.海水中含有钾元素,需经过氧化还原反应才可得到钾单质 |
C和Si两种元素比较,正确的是
| A.在自然界中都有稳定的单质存在 | B.两者的单质在常温下化学性质都很活泼 |
| C.两者的氧化物都能与HF反应 | D.两者的氧化物都是酸性氧化物 |