下列解释事实的离子方程式正确的是
| A.铁和稀硝酸反应制得浅绿色溶液:Fe+ 4H+ + NO3- =Fe3+ + NO↑+ 2H2O |
| B.向Ca(ClO)2溶液中通入过量CO2制取次氯酸: 2ClO-+ H2O + CO2=2HClO + CO32 |
| C.向酸性KMnO4溶液中通入SO2:2MnO4-+5SO2+4OH-=2Mn2++5SO42-+2H2O |
| D.0.01 mol·L—1 NH4Al(SO4)2溶液与0.02 mol·L—1 Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH—=2BaSO4↓+Al(OH)3↓+NH3·H2O |
科学家根据元素周期律和原子结构理论预测,原子序数为114的元素属于第7周期ⅣA族,称为类铅元素。下面关于它的原子结构和性质预测正确的是( )
| A.类铅元素原子的最外层电子数为4 |
| B.其常见价态为+2、+3、+4 |
| C.它的金属性比铅强 |
| D.它的原子半径比铅小 |
A、B分别为第3周期和第4周期的同一主族不同元素的原子,它们原子核内质子数都等于中子数。①若A为ⅡA族,其质量数为x,则B的质子数为y。若A为ⅣA族,其质子数为m,则B的质量数为n。在下列各组值中,y和n的值分别是( )
A.(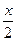 +18)和(2m+18) B.(
+18)和(2m+18) B.(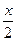 +8)和(2m+8)
+8)和(2m+8)
C.(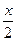 +8)和(2m+36)D.(
+8)和(2m+36)D.(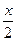 +18)和(2m+18)
+18)和(2m+18)
下列规律错误的是( )
| A.离子半径:F-<Cl-<Br-<I- |
| B.稳定性:HI >HBr>HCl>HF |
| C.还原性:HI>HBr>HCl>HF |
| D.氧化性:F2>Cl2>Br2>I2 |
在一定条件下, 与R-发生如下反应
与R-发生如下反应 +5R-+6H+
+5R-+6H+ 3R2+3H2O,下列有关R元素的叙述正确的是( )
3R2+3H2O,下列有关R元素的叙述正确的是( )
| A.R是第ⅤA族元素 |
| B.R的氢化物水溶液是强酸 |
C. 中的R元素只能被还原 中的R元素只能被还原 |
| D.R2在常温下一定是气体 |
某元素一种同位素原子的质子数为m,中子数为n,则下述论断正确的是( )
| A.不能由此确定该元素的相对原子质量 |
| B.这种元素的相对原子质量为m+n |
| C.若碳原子质量为W克,此原子的质量为(m+n)W克 |
| D.核内中子的总质量小于质子的总质量 |