(15分)甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
已知:①CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+260 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
则CH4与O2反应生成CO和H2的热化学方程式为__________________________;
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。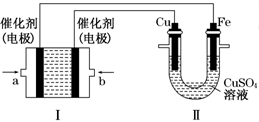
①a处应通入_____(填“CH4”或“O2”),b处电极上发生的电极反应式是______________;
②电镀结束后,装置Ⅰ中KOH溶液的浓度________(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度________;
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH-以外还含有________;
④在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8 g,则装置Ⅰ中理论上消耗氧气________L(标准状况下)。
Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15 ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
| MnO2 |
触摸试管情况 |
观察结果 |
反应完成所需的时间 |
| 粉末状 |
很烫 |
剧烈反应,带火星的木条复燃 |
3.5min |
| 块状 |
微热 |
反应较慢,火星红亮但木条未复燃 |
30min |
(1)写出大试管中发生反应的化学方程式: ,该反应是反应(填放热或吸热)。
(2)实验结果表明,催化剂的催化效果与有关。
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行, 在从0—3分钟各物质的量的变化情况如图所示(A,B,C均为气体)。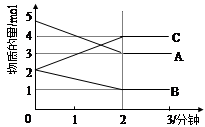
(3)该反应的的化学方程式为;
(4)反应开始至2分钟时,B的平均反应速率为。
(5)能说明该反应已达到平衡状态的是。
a.v(A)= 2v(B) b.容器内压强保持不变
c.v逆(A)= v正(C)d.容器内混合气体的密度保持不变
(6)由图求得A的平衡时的转化率为。
下表为元素周期表的一部分,表中列出了11种元素在周期表中的位置,按要求完成下列各小题。
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
⑥ |
⑦ |
⑨ |
|||||
| 3 |
① |
③ |
⑤ |
⑧ |
⑩ |
|||
| 4 |
② |
④ |
(1)化学性质最不活泼的元素是(填元素符号),其原子结构示意图为 。
(2)元素⑧的名称为,其最高价氧化物的水化物的化学式为。
(3)元素③与元素⑧形成化合物的电子式为 。
(4)非金属性最强的元素是(填元素符号)。除0族外原子半径最大的元素是(填元素符号)。元素①单质与水反应的离子方程式是。
(5)①、③、⑤三种元素的最高价氧化物水化物中,碱性最强的化合物的化学式是。
(6)能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的单质与①的最高价氧化物的水化物反应的化学方程式。
下列物质中:
(1)互为同分异构体的有;
(2)互为同素异形体的有;
(3)属于同位素的有;
(4)属于同一种物质的有。(填序号)
①液氯;② ;③白磷;④氯气;⑤
;③白磷;④氯气;⑤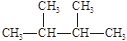 ;⑥
;⑥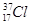 ;⑦
;⑦ ;⑧红磷
;⑧红磷
在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4 2NO2的平衡。下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
2NO2的平衡。下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)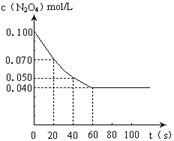
(1)计算在20至40秒时间内,NO2的平均生成速率为mol•L-1•S -1。
(2)①该反应的化学平衡常数表达式为。
②求该温度下平衡常数的值。(写出计算过程,下同)
(3)求达到平衡状态时N2O4的转化率。
(4)求平衡时容器内气体压强与反应前的压强之比为多少?(最简整数比)。
某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。
(1)将上述反应设计成的原电池如图甲所示,请回答下列问题: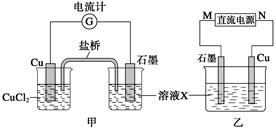

①图中X溶液是;
②石墨电极上发生的电极反应式为;
③原电池工作时,盐桥中的(填“K+”或“Cl-”)不断进入X溶液中。
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是极;②图丙中的②线是的变化。
③当电子转移为2 mol时,向乙烧杯中加入L 5 mol·L-1 NaOH溶液才能使Cu2+沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O Na2FeO4+3H2↑,则电解时阳极的电极反应式是。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是。
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为。