短周期元素A、B、C、D的原子序数依次递增,A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数,D元素原子最外层电子数为电子层数的2倍,四种元素原子的核电荷数之和为36。则下列叙述正确的是
A.C元素的单质在B元素的单质中燃烧,产物1mol与足量的水反应转移电子数为NA
B.由上述元素形成的化合物只有一种具有漂白性
C.B、C、D三种元素形成的化合物的水溶液用惰性电极电解时,溶液pH一定不变
D.A、B形成化合物的沸点高于A、C形成化合物的沸点,因为前者分子间形成了氢键
某温度下,H2(g)+CO2(g) H2O(g)+CO(g)的平衡常数K=2.25。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
H2O(g)+CO(g)的平衡常数K=2.25。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
| 起始浓度 |
甲 |
乙 |
丙 |
| c(H2)/mol/L |
0.010 |
0.020 |
0.020 |
| c(CO2)/mol/L |
0.010 |
0.010 |
0.020 |
下列判断不正确的是
A.反应开始时,反应速率:甲<乙<丙
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,c(CO2)丙=2c(CO2)甲
D.平衡时,乙中CO2的体积分数大于60%
0.100 mL 6 mol·L-1 H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量,可向反应物中加入适量下列物质中的:①硫酸钠固体 ②水 ③硫酸钾溶液 ④硝酸钾溶液 ⑤醋酸钠固体 ⑥硫酸铜固体
| A.②③⑤ | B.①④⑤ | C.②③⑥ | D.③④⑥ |
一定温度下,在恒容密闭容器中发生如下反应:2X(g)+Y(g) 3Z(g),若反应开始时充入2mol X和2mol Y,达平衡后Y的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后Y的体积分数>a%的是
3Z(g),若反应开始时充入2mol X和2mol Y,达平衡后Y的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后Y的体积分数>a%的是
| A.1molY,1molZ | B.2mol X,1molY,1molN2 |
| C.1molY和3molZ | D.2molZ |
对于可逆反应:A2(g)+3B2(g) 2AB3(g)△H >0下列图象中正确的是
2AB3(g)△H >0下列图象中正确的是 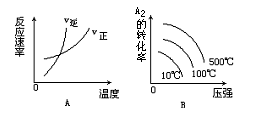
在一容积不变的密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g) 2C(g);△H<0。达到平衡后,只改变一个条件(x),下列量(y)的变化一定符合图中曲线的是
2C(g);△H<0。达到平衡后,只改变一个条件(x),下列量(y)的变化一定符合图中曲线的是
| x |
y |
|
| A |
再加入A |
B的转化率 |
| B |
再加入C |
A的体积分数 |
| C |
增大体积 |
A的转化率 |
| D |
降低温度 |
混合气体的密度 |