某元素X的最高价氧化物的分子式为X2O5,则它的气态氢化物化学式为
| A.XH | B.H2X | C.XH3 | D.XH5 |
同周期的X、Y、Z三元素,其最高价氧化物对应水化物的酸性由弱到强的顺序是:H3ZO4<H2YO4<HXO4,则下列判断正确的是
| A.原子半径:X>Y>Z |
| B.非金属性:X>Y>Z |
| C.阴离子的还原性按X、Y、Z的顺序由强到弱 |
| D.气态氢化物的稳定性按X、Y、Z的顺序由弱到强 |
某CH4燃料电池,工作环境是熔融的金属氧化物(MO),它能传导O2-,有关CH4燃料电池的说法中正确的是
| A.电池内部电子从正极流向负极 |
| B.负极电极反应式为:CH4-8e- + 10OH-=CO32-+ 7H2O |
| C.正极电极反应式为:O2 + 4e-=2O2- |
| D.每消耗22.4 L CH4,外线路中将通过8 mol电子 |
在稀硫酸酸化的H2O2溶液中加入乙醚(C2H5 —O—C2H5 )后,溶液分层,再加入少量K2Cr2O7 溶液,并振荡,在乙醚层中出现深蓝色,这是因为生成2CrO5•(C2H5)2O所致,其反应方程式为:Cr2O72- + 4H2O2+2H+ = 2CrO5 + 5H2O ,已知:CrO5 的结构式为: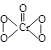 下列说法正确的是
下列说法正确的是
| A.Cr2O72-被氧化成CrO5 | B.该反应为氧化还原反应 |
| C.反应中H2O2被还原成H2O | D.此反应用于检验Cr2O72-离子的存在 |
已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法不正确的是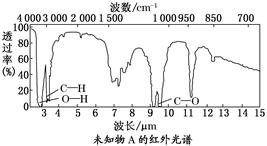

| A.由红外光谱可知,该有机物中至少有三种不同的化学键 |
| B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子 |
| C.仅由核磁共振氢谱无法得知其分子中的氢原子总数 |
D.若 A的化学式为C3H8O,则其结构简式可能为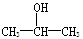 |
分子式为C4H8O3的有机物,在一定条件下具有下列性质:①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应;②在浓硫酸存在下,能生成一种分子式为C4H6O2的五元环状化合物。根据上述性质,确定C4H8O3的结构简式为
| A.HOCH2COOCH2CH3 | B.CH3CH(OH)CH2COOH |
| C.HOCH2CH2CH2COOH | D.CH3CH2CH(OH)COOH |