A+、B2-、C-三种离子具有相同的电子层结构,以下比较中正确的是
| A.原子半径B<C<A | B.原子序数A>B>C |
| C.离子半径B2->C->A+ | D.原子的电子总数C<A<B |
如果3.2 g XO2中含有0.1 mol的氧原子,则X的相对原子质量为( )
| A.32 | B.16 | C.48 | D.8 |
下列说法不正确的是()
| A.64 g氧气中含氧分子数为2NA | B.1.7 g OH-中所含的电子数为NA |
| C.49 g硫酸中所含氧原子数为2NA | D.58.5 g氯化钠中所含的离子数为NA |
下列叙述正确的是( )
| A.1 mol OH-的质量为17 g |
| B.CO2的摩尔质量为44 g |
| C.Fe原子的摩尔质量等于它的相对原子质量 |
D.1个Na原子的质量等于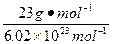 |
下列有关阿伏加德罗常数(NA)的描述正确的是( )
| A.1 mol物质均约含有6.02×1023个分子 |
| B.NA个氢气分子就是1 mol H2 |
| C.1 g氢气约含有6.02×1023个分子 |
| D.NA个12C的质量为12 g |
下列说法正确的是( )
| A.摩尔是物理量之一 |
| B.某物质含有6.02×1023个粒子,这种物质的物质的量就是1 mol |
| C.1 mol氧 |
| D.1 mol KClO3和1 mol SO2中,所含氧原子的个数比为3∶2 |