请按要求回答下列问题。
(1)根据下图回答①②。
①打开K2,闭合K1。A极电极反应式为_________________,B极的现象____________。
②B极重新换根碳棒,再打开K1,闭合K2。
B极电极反应式_______________________________。
装置发生的总反应化学方程式______________。实验完成后,锌电极增重a g,则阳极产生标准状况下的气体体积_____ ___L。
(2)改变两电极的电极材料,利用该装置要实现Cu+H2SO4== CuSO4+H2↑反应的发生,应打开____闭合_____,其电解质溶液需用 ,B电极材料是用 ,A电极反应式为 。
(7分)A、B、C、D四种烃分子中均含有8个氢原子,其中A、B常温下呈气态, C 、D呈液态。
(1)A是符合上述条件中相对分子质量最小的,则A的分子式为▲;
(2)B属于链状单烯烃,且与HBr加成的产物只有一种,试写出B与HBr反应的化学方程式▲。
(3)C属于芳香烃,1mol C最多能和3molH2加成,试写出C的结构简式▲。
(4)已知: ;
;
烃D存在如下转化关系: (唯一产物)
(唯一产物)
试写出D的结构简式▲。
(8分)有人设想合成具有以下结构的烃分子.
(1)结构D显然是不可能合成的,原因是 ▲.
(2)在结构A的每两个碳原子之间插入一个CH2原子团,可以形成金刚烷的结构,金刚烷的分子式为 ▲
(3)B的一种同分异构体是最简单的芳香烃,能证明该芳香烃中的化学键不是单双键交替排列的事实是 ▲
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
(4)C的一种属于芳香烃的同分异构体是生产某塑 料的单体,写出合成该塑料的化学方式 ▲
料的单体,写出合成该塑料的化学方式 ▲
(9分)根据要求填空:
(1)写出下列有机物的键线式: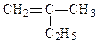 _____▲ ______CH3CH2CH2COOH __▲ _______
_____▲ ______CH3CH2CH2COOH __▲ _______
(2)写出有机物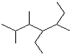 的名称 ▲
的名称 ▲
(3)写出下列原子团的电子式:①甲基 ▲②氢氧根离子 ▲
(4)在有机物分子中若某一个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”。C7H16的同分异构体中具有“手性碳原子”的有___▲ ____种.
(5)某有机高分子化合物的结构片段如下: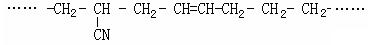
则合成它的单体是▲、▲、▲
为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒剂、漂白剂等。
(1) 过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠有发生了还原反应的是
| A.MnO2 | B.KMnO4溶液 | C.Na2SO3溶液 | D.稀硫酸 |
(2) 漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。当生成1m olClO2时转移的电子数是
olClO2时转移的电子数是
(3) 二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与SO2反应制得。请写出反应的离子方程式:
(4)有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,则该反应中还原剂与氧化剂的物质的量之比为
(1)某化学反应可用下式表示:A + B ="=" C + D + H2O ,若A、D均可用于消毒,且C是家家户户的厨房必备的物质之一,写出该反应的离子方程式:
(2)硝酸铅的稀溶液中,滴入几滴稀 生成白色
生成白色 沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式①②
沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式①②
(3)边微热边向铵明矾[NH4Al(SO4)2`12H2O]溶液中逐滴加入 溶液至中性(提示:NH+ 4、Al3+恰好完全反应)
溶液至中性(提示:NH+ 4、Al3+恰好完全反应)
①此时发生反应的离子方程式为
②向以上所得中性溶液中继续滴加稀硫酸,相关反应的离子方程式是: