下列说法中正确的是
A.常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(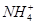 )、c(H+)均下降 )、c(H+)均下降 |
B.常温下,c(N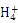 )相等的①(NH4)2SO4②(NH4)2Fe(SO4)2③NH4Cl④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ )相等的①(NH4)2SO4②(NH4)2Fe(SO4)2③NH4Cl④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ |
| C.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
D.当溶液中存在的离子只有Cl-、OH-、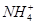 、H+时,该溶液中离子浓度大小关系可能为c(Cl-)>c( 、H+时,该溶液中离子浓度大小关系可能为c(Cl-)>c(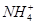 )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
进行如下实验,在A锥形瓶中放入10g块状CaCO3,在B锥形瓶中放入5g粉末状CaCO3,分别加入50mL2mol/L盐酸。下图中能正确表示实验结果的是()
某同学按下图所示的装置进行电解实验。下列说法正确( )

| A.电解过程中,铜电极上有H2产生 |
| B.电解过程中,铜电极不断溶解 |
| C.电解过程中,石墨电极上始终有铜析出 |
| D.整个电解过程中,H+的浓度不断增大 |
能正确反映出N2+3H2 2NH3,△H<0的关系的是( )
2NH3,△H<0的关系的是( )
化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在常温下,下列反应的平衡常数的数值如下:
2NO(g) N2(g)+O2(g) K1=1×1030
N2(g)+O2(g) K1=1×1030
2H2(g)+O2(g) 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081
2CO2(g) 2CO(g)+O2(g) K3=4×10-92
2CO(g)+O2(g) K3=4×10-92
以下说法正确的是( )
| A.常温下,NO分解产生O2的反应的平衡常数表达式为K1=c(N2)·c(O2) |
| B.常温下,水分解产生O2,此时平衡常数的数值约为5×10-80 |
| C.常温下,NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2 |
| D.以上说法都不正确 |
下列说法不正确的是
| A.钢铁发生电化学腐蚀时,负极发生的反应是2H2O+O2+4e-=" 4" OH- |
| B.在空气中,金属铝表面能迅速被氧化形成保护膜,因此铝不容易被腐蚀 |
| C.铸铁输油管道应埋在干燥致密不透气的土壤中 |
| D.白铁(镀Zn铁)表面有划损时,也能阻止铁被氧化 |