(本题15分)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途.请回答以下问题:
(1)Cu+基态核外电子排布式为
(2)与OH-互为等电子体的一种分子为 (填化学式)。
(3)氯和钾与不同价态的铜可生成两种化合物,其阴离子均为无限长链结构(如图),a位置上Cl原子的杂化轨道类型为__________。已知其中一种化合物的化学式为KCuCl3,另一种的化学式为___________;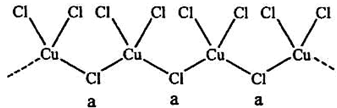
(4)Cu2O的熔点比Cu2S的 (填“高”或“低”),请解释原因_________。
(5)一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是________;
(6)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为__________。
(7)将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4作催化剂,即发生反应,生成硫酸铜。其反应过程的第2步是:2Fe3++Cu===2Fe2++Cu2+,请写出其第l步反应的离子方程式__________________________________。
I下列有关叙述正确的是
| A. |
碱性锌锰电池中, 是催化剂 |
| B. |
银锌纽扣电池工作时, 被还原为 |
| C. |
放电时,铅酸蓄电池中硫酸浓度不断增大 |
| D. |
电镀时,待镀的金属制品表面发生还原反应 |
Ⅱ锌是一种应用广泛的金属,目前工业上主要采用"湿法"工艺冶炼锌。某含锌矿的主要成分为
(还含少量
等其他成分),以其为原料冶炼锌的工艺流程如图所示:
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为。
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的操作.
(3)浸出液"净化"过程中加入的主要物质为,其作用是。
(4)电解沉积过程中的阴极采用铝板,阳极采用
合金惰性电极,阳极逸出的气体是。
(5)改进的锌冶炼工艺,采用了"氧压酸浸"的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质。"氧压酸浸"中发生的主要反应的离子方程式为。
(6)我国古代曾采用"火法"工艺冶炼锌。明代宋应星著的《天工开物》中有关于 "升炼倭铅"的记载:"炉甘石十斤,装载入一泥罐内,……,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……,冷淀,毁罐取出,……,即倭铅也。"该炼锌工艺过程主要反应的化学方程式为。(注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌)
【选修3-物质结构与性质】
I 对于钠的卤化物(
)和硅的卤化物(
),下列叙述正确的是()
| A. | 难水解 | B. | 是共价化合物 |
| C. | 易水解 | D. | 的熔点一般高于 |
Ⅱ碳元素的单质有多种形式,下图依次是
、石墨和金刚石的结构图: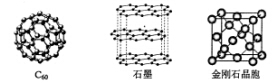
回答下列问题:
(1)金刚石、石墨、
.碳纳米管等都是碳元素的单质形式,它们互为。
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为、。
(3)
属于晶体,石墨属于晶体。
(4)石墨晶体中,层内C-C键的键长为142
,而金刚石中C-C键的键长为154
。其原因是金刚石中只存在
-
间的共价键,而石墨层内的
-
间不仅存在共价键,还有键。
(5)金刚石晶胞含有个碳原子。若碳原子半径为
,金刚石晶胞的边长为
,根据硬球接触模型,则
=
,列式表示碳原子在晶胞中的空间占有率(不要求计算结果)。
I图示为一种天然产物,具有一定的除草功效。下列有关该化合物的说法错误的是

A.分子中含有三种含氧官能团
B.1
该化合物最多能与6
反应
C.既可以发生取代反应,又能够发生加成反应
D.既能与
发生显色反应,也能和
反应放出
Ⅱl,6-己二酸(
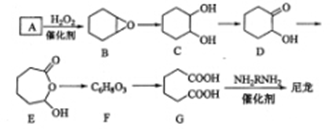
)是合成尼龙的主要原料之一,可用含六个碳原子的有机化合物氧化制备。下图为
通过氧化反应制备
的反应过程(可能的反应中间物质为
、
、
、
和
):
回答下列问题:
(1)化合物
中含碳87.8%,其余为氢,
的化学名称为。
(2)
到
的反应类型为。
(3)
的结构简式为。
(4)在上述中间物质中,核磁共振氢谱出峰最多的是,最少的是。(填化合物代号)
(5)由
合成尼龙的化学方程式为。
(6)由
通过两步反应制备1,3-环己二烯的合成路线为。
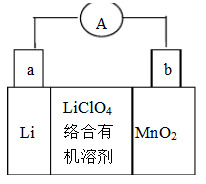
锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质
。溶于混合有机溶剂中,
通过电解质迁移入
晶格中,生成
。
回答下列问题:
(1)外电路的电流方向是由极流向极。(填字母)
(2)电池正极反应式为。
(3)是否可用水代替电池中的混合有机溶剂?(填"是"或"否"),原因是。
(4)
可与
和
,在高温下反应,生成
,反应的化学方程式为。
在酸性溶液中歧化,生成
和
的物质的量之比为。
卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多卤代甲烷作为溶剂,其中分子结构为正四面体的是。工业上分离这些多卤代甲烷的方法是。
(2)三氟氯溴乙烷(
)是一种麻醉剂,写出其所有同分异构体的结构简式(不考虑立体异构)。
(3)聚氯乙烯是生活中常见的塑料。工业生产聚氯乙烯的一种工艺路线如下:
反应①的化学方程式是,反应类型为,反应②的反应类型为。