已知:CO2(g) + C(s) =2CO(g) ΔH1
C(s) + H2O(g) = CO(g) + H2(g) ΔH2
CO(g) + H2O(g) =CO2(g) + H2(g) ΔH3
CuO(s) + CO(g) =Cu(s) + CO2(g) ΔH4
2CuO(s) + C(s) =2Cu(s) + CO2(g) ΔH5
下列关于上述反应焓变的判断不正确的是
| A.ΔH1 >0 | B.ΔH2 >0 |
| C.ΔH2<ΔH3 | D.ΔH5= 2ΔH4 +ΔH1 |
设NA为阿伏加德罗常数,下列有关叙述不正确的是( )
| A.常温常压下,1 mol碳烯(∶CH2)所含电子总数为8NA |
B.在标准状况下,V L水中含有的氧原子个数为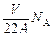 |
| C.常温时,1 L pH = 1的水溶液中水合氢离子数为0.1 NA |
| D.1 mol OH –在电解过程中被氧化,提供电子的数目为NA |
设NA为阿伏加德罗常数,则下列说法错误的是()
| A.5.6gFe 与足量的氯气反应时失去的电子数目为0.2NA |
| B.0.1molN5+离子中所含的电子数为3.4NA |
| C.1 L0.2mol/L氯化钡溶液中含氯离子的数目为0.4NA |
| D.在标准状况下,11.2LSO3所含原子数目大于2NA |
下列各组溶液,不用其它试剂。就可以将它们区别开的是( )
| A.盐酸氢氧化钠碳酸钠硫酸钠 |
| B.盐酸硝酸铵氢氧化钠硝酸钠 |
| C.氢氧化钠硝酸镁碳酸钠 硫酸氢钠 |
| D.氯化钡硫酸钠氯化钙 硝酸钙 |
为了除去C02中的02、S02、H20(g)等杂质,可用①NaHC03饱和溶液②浓硫酸③加热的铜网,通过以上试剂顺序净化效果最好的是 ( )
| A.②③① | B.③②① | C.②①③ | D.①②③ |
下列各项操作中,能发生“先沉淀后溶解”现象的是 ( )
| A.向饱和Na2CO3溶液中通入过量的CO2 |
| B.向Fe(OH)3胶体中逐滴滴入过量的稀H2SO4 |
| C.向AlCl3溶液中通入过量的NH3 |
| D.向CaCl2溶液中通入过量的CO2 |