(16分)物质的类别和核心元素的化合价是研究物质性质的两个基本视角。
(1)图中X的电子式为 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O (填“强”或“弱”)。用原子结构解释原因:同主族元素最外层电子数相同,从上到下, ,得电子能力逐渐减弱。
(2)Na2S2O3是一种用途广泛的钠盐。
①下列物质用于Na2S2O3的从氧化还原反应的角度制备, ,理论上有可能的是 (填字母序号)。
a.Na2S+S b.Z+S c.Na2SO3+Y d.NaHS+NaHSO3
②已知反应:Na2S2O3+H2SO 4Na2SO4+S↓+SO2↑+H2O。研究其反应速率时,下列说法正确的是 (填写字母序号)。
4Na2SO4+S↓+SO2↑+H2O。研究其反应速率时,下列说法正确的是 (填写字母序号)。
a.可通过测定一段时间内生成SO2的体积,得出该反应的速率
b.可通过比较出现浑浊的时间,研究浓度、温度等因素对该反应速率的影响
c.可通过Na2S2O3固体与稀硫酸和浓硫酸的反应,研究浓度对该反应速率的影响
(3)治理含CO、SO2的烟道气,可以将其在催化剂作用下转化为单质S和无毒的气体。
①已知:CO(g)+1/2O2(g)=CO2(g) △H=-283kJ·mol-1
S(s)+O2(g)=SO2(g) △H=-296kJ·mol-1
则治理烟道气反应的热化学方程式为 。
②一定条件下,将CO与SO2以体积比为4∶1置于恒容密闭容器中发生上述反应,下列选项能说明反应达到平衡状态的是 (填写字母序号)。
a.v(CO)∶v(SO2)=2∶1
b.平衡常数不变
c.气体密度不变
d.CO2和SO2的体积比保持不变
测得上述反应达平衡时,混合气体中CO的体积分数为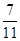 ,则SO2的转化率为 。
,则SO2的转化率为 。
(4)最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。甲醇可制作燃料电池。写出以氢氧化钾为电解质的甲醇燃料电池负极反应式 。
(5)某同学用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得一些物质在20℃的数据如下表。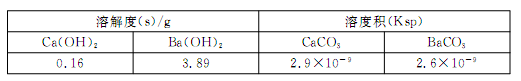
吸收CO2最合适的试剂是 (填“Ca(OH)2”或“Ba(OH)2”)溶液。
在相同状况下,一个空瓶,若装满O2称其质量为36 g,若装满CO2称其质量为42 g,若装满A气体,称其质量为52 g,则A的相对分子质量是____________
在标准状况下4.48L CH4和CO2混合气体的质量为6.0g,则混合气体平均摩尔质量为 g/mol,相对于氢气的密度为 ;CH4和CO2的质量比为 .
O2和O3是氧元素的两种单质,根据其化学式完成下列各题:
①等质量的O2和O3所含分子个数比为________,原子个数比为________,分子的物质的量之比为________。
②等温等压下,等体积的O2和O3所含分子个数比为________,原子个数比为________,质量比为________。
在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)。体系中,n(NO)随时间的变化如表:
2NO2(g)。体系中,n(NO)随时间的变化如表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)(mol) |
0.020 |
0.01. |
0.008 |
0.007 |
0.007 |
0.007 |
(1)写出该反应的平衡常数表达式:K= 。
已知: >
> ,则该反应是 热反应。
,则该反应是 热反应。
(2)图中表示NO2的变化的曲线是 。
用O2表示从0~2 s内该反应的平均速率v= 。
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(一) A和B反应生成C,假定反应由A、B开始,它们的起始浓度均为1mol/l。反应进行2min后A的浓度为0.8mol/l, B的浓度为0.6mol/l, C的浓度为0.6mol/l。则2min内反应的平均速率为v(A)= ,v (B) = ,v(C)= 。该反应的化学反应方程式为: 。
(二) 比较下列各组热化学方程式中的ΔH的大小关系。
(1)已知1 mol白磷转化成红磷,放出18.39 kJ的热量,又知:①P4 (白,s)+5O2(g)=2P2O5(s) ΔH1,
②4P(红,s)+5O2(g)=2P2O5(s) ΔH2。
则ΔH1和ΔH2的关系:ΔH1 ΔH2
(2)③ S(g)+O2(g)==SO2(g) △H1
④S(s)+O2(g)==SO2(g) △H2 ΔH1 ΔH2
(3)已知:高温下,在密闭容器中用H2还原WO2可得到金属钨。当温度过高时,WO2(s)会转变为WO2 (g)。请根据以下反应:
⑤WO2 (s) + 2H2 (g)  W (s) + 2H2O (g) ΔH = +66.0 kJ· mol-1
W (s) + 2H2O (g) ΔH = +66.0 kJ· mol-1
⑥WO2 (g) + 2H2 W (s) + 2H2O (g) ΔH = -137.9 kJ· mol-1
W (s) + 2H2O (g) ΔH = -137.9 kJ· mol-1
计算出WO2 (s)  WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。