下列叙述不正确的是
| A.根据某元素原子的质子数和中子数,可以确定该元素的相对原子质量 |
| B.CaCl2、MgCl2晶体都容易潮解,它们潮解的实质是晶体表面吸水形成溶液 |
| C.根据金属活动性顺序表,可以推断冶炼金属时可能的方法 |
| D.根据酸、碱、盐的溶解性表,可以判断某些溶液中的复分解反应能否进行 |
乙醇分子结构中各种化学键如下所示,关于乙醇在各种反应中断键的说明不正确的为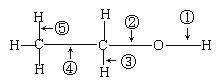
| A.和乙酸共热时,断裂①键 |
| B.和金属钠反应时,键①断裂 |
| C.和P2O5共热时,键②⑤断裂 |
| D.在铜催化下和氧气反应时,键①⑤断裂 |
设阿伏加德罗常数的值为NA,下列说法中正确的是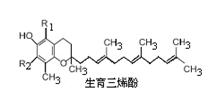
A.1mol苯乙烯( )中含有的碳碳双键数为4NA )中含有的碳碳双键数为4NA |
| B.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| C.0.1molCnH2n+2中含有的碳碳单键数为0.1n NA |
| D.标准状况下,2.24LCHCl3含有的分子数为0.1NA |
有四种有机物①(CH3)2CHCH(CH3)2,②(CH3)2C(CH3)2,③CH3(CH2)2CH(CH3)2,④CH3CH2C(CH3)3有关此四物质的下列叙述正确的是
| A.①和②互为同分异构体,①和④互为同系物 |
| B.④的一氯代物有四种 |
| C.②可以由烯烃与氢气加成而获得 |
| D.能通过加氢反应得到③的炔烃有2种 |
右图是一个氢核磁共振谱,请你观察图谱,分析其可能是下列物质中
| A.CH3CH2CH2CH3 | B.(CH3)2CHCH3 |
| C.CH3CH2CH2OH | D.CH3CH2COOH |
下列化学用语正确的是:
A.聚丙烯的结构简式为: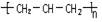 |
B.丙烷分子的球棍模型为: |
C.四氯化碳分子的电子式为: |
D.TNT的结构简式为: |