为测定碱式碳酸钴[COx(OH)y(CO3)z]的化学组成,研究性学习小组的同学设计了如图所示的装置进行实验探究。已知:碱式碳酸钴受热时可分解生成三种氧化物。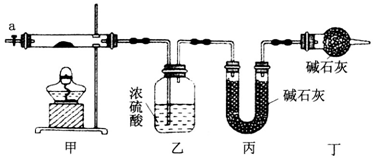
(1)按如图所示装置组装好仪器,并___________;称取3.65g样品置于硬质玻璃管内,加热,当乙装置中_______(填实验现象),停止加热;打开活塞a,缓缓通入空气数分钟,通入空气的目的是__________。
(2)某同学认为上述实验中存在一个缺陷,该缺陷是_________。
(3)通过正确实验测得乙、丙装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为__________。
(4)CoCl2·6H2O常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取COCl2·6H2O的一种工艺如下: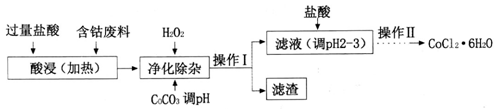
已知:25℃时
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
CO(OH)2 |
Al(OH)3 |
| 开始沉淀(pH) |
2.3 |
7.5 |
7.6 |
3.4 |
| 完全沉淀(pH) |
4.1 |
9.7 |
9.2 |
5.2 |
①净化除杂时,加入H2O2发生反应的离子方程式为______________;
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为_________;
③加盐酸调整pH为2~3的目的为___________;
④操作Ⅱ过程为蒸发浓缩、冷却结晶、过滤。
乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4·xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定。学习小组的同学设计了滴定的方法测定x值。
①称取2.520 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.100 0 mol·L-1的KMnO4标准溶液进行滴定,达到终点时消耗20.00 mL。
(1)写出草酸(H2C2O4)与酸性高锰酸钾溶液反应的化学方程式____________。
(2)滴定时,将酸性KMnO4标准液装在如图中的________(填“甲”或“乙”)滴定管中。
(3)本实验滴定达到终点的标志是__________。
(4)通过上述数据,求得x=________。
讨论:①若滴定终点时仰视滴定管刻度,则由此测得的x值会_______(填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会________。
随着科学技术的发展,阿伏加德罗常数的测定手段越来越多,测定的精度也越来越高。现有一种简单可行的测定方法,具体步骤为:
①准确称取mg干燥后的NaCl固体细粒并转移到定容仪器A中;
②用滴定管向A仪器中加苯,不断振荡,继续加苯到A仪器的刻度,
计算出NaCl固体的体积V cm3。
(1)步骤①中仪器A最好使用_______________(填序号)
| A.量筒 | B.烧杯 | C.容量瓶 | D.试管 |
(2)步骤②中是否用酸式滴定管还是用碱式滴定管_____________,理由是__________。
(3)能否用水代替苯_________,理由是_____________________。
(4)已知NaCl晶体中,靠得最近的Na+、Cl-间的距离为a cm(如图),则用上述方法测得的阿伏加德常数NA的表达式为_______________。
如图是某研究性学习小组设计制取氯气并以氯气为原料进行特定反应的装置.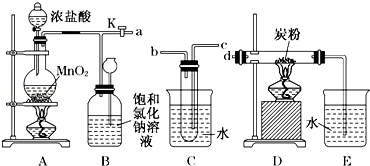
(1)写出A装置中发生反应的离子方程式_________;要将C装置接入B和D之间,正确的接法是:
a→ → →d;
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯,Cl2通过C装置后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为________.
(3)D处反应完毕后,关闭旋塞K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是 ,B的作用是 .
(4)用量筒量取20mL E中溶液,倒入已检查完气密性良好的分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡,静置于铁架台上(如图),等分层后取上层液和下层液,呈黄绿色的是 (填“上层液”或“下层液”),能使有色布条褪色的是 (填“上层液”或“下层液”).
(5)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由并在方框中画出改进后的装置图.
某化学兴趣小组用下图所示装置进行电化学原理的实验探究,试回答下列问题:
(1)通O2的Pt电极为电池 极(填电极名称),其电极方程式为 。
(2)若B电池为电镀池,目的是在某镀件上镀一层银,则X电极材料为 ,电解质溶液为 。
(3)若B电池为精炼铜,且粗铜中含有Zn、Fe、Ag、Au等杂质,则该电池阳极泥的主要成分是 。
(4)若B电池的电解质溶液为500 mL 1.0mol/L的NaCl溶液,X、Y皆为惰性电极,当电池工作一段时间断开电源K,Y电极有560mL(标准状况)无色气体生成(假设电极产生气体完全溢出,溶液体积不变),此时B电池溶液的pH= ,要使该溶液恢复到原来的状态,需加入 (填物质并注明物质的量)。
(5)若X、Y均是铜,电解质溶液为NaOH溶液,电池工作一段时间,X极附近生成砖红色沉淀,查阅资料得知是Cu2O,试写出该电极发生的电极反应式为 。
某课外活动小组的同学对“菠菜与豆腐同食会引起结石”的说法产生了兴趣。于是查阅了相关资料,并进行了实验操作欲检测菠菜中草酸盐的含量。查阅资料得知:
Ⅰ. 菠菜中富含可溶性草酸盐,易与豆腐中的钙盐形成不溶于水能溶于稀硫酸的草酸钙(CaC2O4)
Ⅱ. 有关专家建议食用高草酸蔬菜的同时,适当摄入高钙食物,使二者在肠道内结合成草酸钙沉淀,并随着大便排出体外。以免草酸进入血液中与人体内的血钙结合,形成血液中的草酸钙需经肝脏、肾脏、尿道,随着小便排出体外,大量草酸钙流经肾脏,提升了泌尿系统结石的风险。
Ⅲ. 草酸(H2C2O4)具有较强的还原性。回答下列问题:
(1)该活动小组的同学取m g菠菜样品在研钵中研磨成汁,用足量热的稀硫酸溶液浸泡,最后 (填操作名称)得到澄清溶液。
(2)将溶液转入容量瓶中并加水配制成250mL溶液A。
(3)用滴定法测定草酸盐的含量。
①量取待测溶液A 20.00 mL于锥形瓶中,置于铁架台的白纸上。
②用 (填仪器名称)盛装0.1000mol/LKMnO4标准溶液进行滴定时:眼睛注视 ;当 时,停止滴定,并记录KMnO4标准溶液的终读数。重复滴定3次。
(4)KMnO4滴定待测溶液A时发生反应的离子方程式为 ,根据下表实验数据计算菠菜中草酸盐(以C2O42-计算)的质量分数为(可以只列式不化简) 。
| 滴定次数 |
待测溶液A的体积(mL) |
KMnO4标准溶液的体积 |
|
| 滴定前的刻度(mL) |
滴定后的刻度(mL) |
||
| 第一次 |
20.00 |
0.10 |
20.12 |
| 第二次 |
20.00 |
2.20 |
24.20 |
| 第三次 |
20.00 |
4.30 |
24.28 |
(5)下列操作会使测定结果偏高的是 。
A.配制溶液时未洗涤烧杯和玻璃棒
B.锥形瓶未干燥就直接加入待测液
C.未用标准液润洗盛装标准液的仪器就加入标准液开始滴定
D.滴定前尖嘴处有气泡滴定后气泡消失
E.滴定后俯视读数