化学实验有助于理解化学知识,提升科学素养。某学习小组在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关探究。
(1)已知发生装置如图所示。请写出该反应的离子方程式 。
制备实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)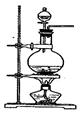
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加入浓盐酸
(2)为了制取纯净干燥的氯气,应将氯气依次通过盛有 , 的试剂瓶(填试剂名称)
(3)该小组关于实验中可制得氯气体积(标准状况)的讨论正确的是 。
A.若提供0.4 mol HCl,MnO2不足量,则可制得氯气2.24 L
B.若提供0.4 mol HCl,MnO2过量,则可制得氯气2.24 L
C.若有0.4 mol HCl参与反应,则可制得氯气2.24 L
D.若有0.4 mol HCl被氧化,则可制得氯气2.24 L
(4)写出工业制氯气的化学方程式
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉,这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”。请分别用如图所示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6 mol·L-1的盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去。)
填写下列空白:
(1)实验进行时试管A中应加入的试剂是_________________;烧瓶B的作用是____________;烧瓶C的作用是_______________
(2)实验时,长颈漏斗H中应加入_____________________U型管G的作用是____________
(3)装置I中,在实验时需要加热的仪器是(填该仪器对应的字母)_____________ ;
当反应转移了4mol电子时,试管D中收集到的气体在标准状况下的体积为_____________。
(4)写出试管A中发生反应的化学方程式:________________________
50ml0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程 中放出的热量可计算中和热。回答下列问题: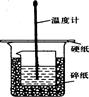
(1)烧杯间填满碎纸条的作用是 。
(2)从实验装置上看,图中缺少的仪器是 。
(3)实验中若用70mL0.50mol·L-1盐酸跟70mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”).
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会(填“偏大”“偏小”或“无影响”)。
由于Fe(OH)2极易被氧化;所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。若用图所示实验装置则可制得纯净的Fe(OH)2沉淀。两极材料分别为石墨和铁。
(1)a电极材料为________,其电极反应式为_______________.
(2)电解液d可以是________,则白色沉淀在电极上生成;也可以是________,则白色沉淀在两极之间的溶液中生成。(填字母代号)
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)液体c为苯,其作用是:;在加入苯之前,对d溶液进行加热煮沸处理的目的是:.
(4)为了在短时间内看到白色沉淀,可以采取的措施是。
A.改用稀硫酸做电解液
B.适当增大电源电压
C.适当缩小两电极间距离
D.适当降低电解液温度
(5)若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源,继续电解,除了电极上看到气泡外,另一明显现象为:.
写出反接后两极的电极反应式:
阳极:
阴极:
实验室欲用NaOH固体配制1.0 mol/L的NaOH溶液240 mL。
(1)配制溶液时,一般可以分为以下几个步骤:
①称量②计算③溶解④摇匀⑤移液⑥洗涤⑦定容⑧冷却⑨摇动
其正确的操作顺序为____________________(填序号)。本实验必须用到的仪器有托盘
天平、药匙、玻璃棒、烧杯、_______、。
(2)某同学欲称量NaOH的质量,先用托盘天平称量烧杯的质量,托盘天平平衡后的状
态如图所示。烧杯的实际质量为________g,要完成本实验该同学应称量________g NaOH。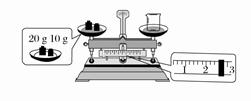
(3)使用容量瓶前必须进行的一步操作是 。
(4)配制过程中,下列操作会引起所配溶液浓度偏高的是
| A.转移溶液时,有少量溶液洒到容量瓶外面 |
| B.定容时俯视刻度线 |
| C.未冷却至室温就将溶液移入容量瓶中并定容 |
| D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加蒸馏水至刻度线 |
Na2S2O3是重要的化工原料,易溶于水。在中性或碱性环境中稳定。
I.制备Na2S2O3•5H2O反应原理:Na2SO3(aq)+S(s) Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15g Na2SO3加入圆底烧瓶中,再加入80ml蒸馏水。另取5g研细的硫粉,用3ml乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分加持装置略去),水浴加热,微沸60分钟。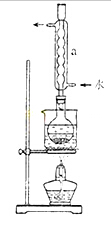
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3•5H2O,经过滤,洗涤,干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是。
(2)仪器a的名称是。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是,检验是否存在该杂质的方法是。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示产品发黄的原因。
II.测定产品纯度准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L‾1碘的标准溶液滴定。反应原理为:2S2O32‾+I2=S4O62-+2I‾
(5)滴定至终点时,溶液颜色的变化:。
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为mL。产品的纯度为(设Na2S2O3•5H2O相对分子质量为M)。