下表是元素周期表的一部分,回答下列问题(答题时用具体元素符号表示)。
| ① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |
② |
|
|
|
|
|
|
|
|
|
|
|
③ |
④ |
⑤ |
|
|
| ⑥ |
|
|
|
|
|
|
|
|
|
|
|
⑦ |
|
|
|
⑧ |
|
| |
|
|
|
|
|
|
⑨ |
|
|
⑩ |
|
|
|
|
|
|
|
(1)①、③形成的6原子气态化合物中含 个σ键, 个π键。
(2)元素⑨的原子核外次外层电子数为 个。焊接钢轨时,常利用元素⑨的氧化物与⑦的单质在高温下发生反应,写出其中一种反应的化学方程式 。
(3)④、⑤两元素原子第一电离能较大的是 ,两元素以质量比7:12组成的化合物A是一种高效火箭推进剂,相对分子质量为152,A的分子式为 。
(4)⑥和⑧可形成某离子化合物,下图所示结构 (选填“能”或“不能”)表示该离子化合物的晶胞;下图所示结构中,X离子的堆积方式为 (选填“ABAB…”或“ABCABC…”)。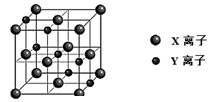
(5)元素⑩单质的晶胞如图所示,该晶胞中金属原子的配位数为 ,每个晶胞“实际”拥有的原子数是 。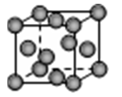
20℃时,醋酸的电离平衡常数为1.6×10-5。
(1)试计算20℃时0.01mol•L-1的醋酸溶液中氢离子浓度。
(2)室温时,向0.2mol•L-1的醋酸溶液中加入等体积的0.1mol•L-1的NaOH(aq),充分反应后所得溶液的PH=4,则:
①所得溶液中各离子(包括CH3COOH分子)浓度大小关系是:______________________,
②所得溶液中的物料守恒式为:________+________=__________=_________mol•L-1。
③c(CH3COOH)=_____________mol•L-1(写出算式,不做近似计算)
将镁铝的混合物0.1mol溶于100ml 2mol/L硫酸溶液中,然后再滴加1mol/L的NaOH溶液,请回答:
(1)若在滴加NaOH溶液过程中,沉淀质量随加入NaOH溶液的体积变化如图所示,当V1=160mL时,则金属粉末中n(Mg)=mol, V2=mL,
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积 V(NaOH) =mL
V(NaOH) =mL
(3)图像中A点的意义是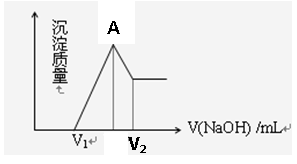
已知在含HNO3的溶液中放入Al不生成H2。某无色透明溶液跟金属铝反应放出H2。试判断下列离子:Mg2+、Cu2+、Ba2+、H+、Ag+、SO32-、SO42-、HCO3-、OH-、NO3-,在下列两种情况下何者能存在于溶液中。
(1)当生成Al3+时,可能大量存在_________________________________________________。
(2)当生成 时,可能大量存在_______________________________________________。
时,可能大量存在_______________________________________________。
取两等份铝粉,第一份加入250 mL 2 mol·L-1的盐酸,第二份加入400 mL2mol·L-1的烧碱。若同温同压下放出气体体积之比为5:6,则加入的铝粉每份质量为。
(10分) 将0.1 mol的镁、铝混合物溶于100 mL 2mol/LH2SO4溶液中,然后再滴加1 mol/L NaOH溶液。请回答:
⑴若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如右图所示。当V1=140mL时,则金属粉末中n(Mg)= mol,V2= mL。
⑵若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH) mL。
⑶若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入480 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:
(4)若滴加NaOH溶液致V2ml时,停止滴加NaOH溶液,开始往溶液中通入足量CO2,请写出发生反应的离子方程式——————————————————————-————。