根据所学知识回答下列问题,在如图所示装置中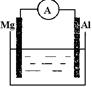 ,
,
(1)若烧杯中溶液为稀硫酸,则观察到的现象为 ,正极反应式为 ,负极反应式为 ,
该装置中的能量变化形式为 。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为 。
化学式为C8Hn的烷烃,m值等于;CnH22的烷烃,n值等于;相对分子质量为212的烷烃的分子式为。
茉莉花是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯: 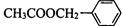 是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
⑴写出反应①的化学方程式:。
⑵反应③的反应类型为。
⑶反应(填序号)原子的理论利用率为100%,符合绿色化学的要求。
⑷C的结构简式为,C通常有三种不同类别的芳香族同分异构体,试写出另两种不同类别的同分异构体的结构简式(各写一种)。
830K时,在密闭容器中发生下列可逆反应:
CO(g)+H2O(g) CO2(g)+H2(g);△H<0试回答下列问题:
CO2(g)+H2(g);△H<0试回答下列问题:
(1)若起始时c(CO)="2" mol•L-1,c(H2O)="3" mol•L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=.
(2)在相同温度下,若起始时c(CO)="1" mol•L-1,c(H2O)="2" mol•L-1,反应进行一段时间后,测得H2的浓度为0.5 mol•L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正)v(逆)(填“大于”“小于”或“等于”),你判断的依据是
。
(3)若降低温度,该反应的K值将(均填“增大”“减小”或“不变”)。
已知某物质A有如下转化关系: 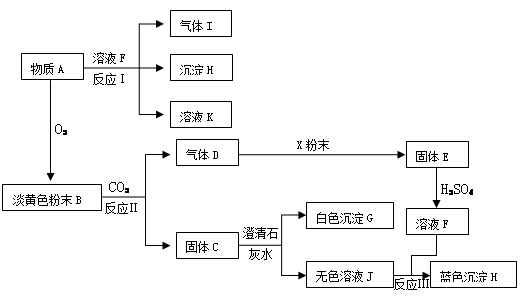
根据上图关系及实验现象,回答下列问题:
(1)A是,B是,G是,X是(均填化学式)。
(2)写出反应Ⅱ的化学方程式。
(3)写出反应Ⅲ的离子方程式。
钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
。
(2)下列可防止铁棒被腐蚀装置是。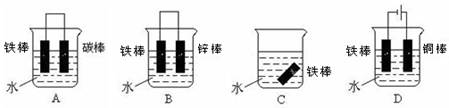
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下: 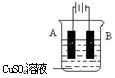
请回答:A电极对应的金属是______(写元素名称),B电极的电极反应式是。
镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
。