已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
| A.AgCl>AgI>Ag2CrO4 | B.AgCl>Ag2CrO4>AgI |
| C.Ag2CrO4>AgCl>AgI | D.Ag2CrO4>AgI>AgCl |
由以下五种基团两两结合而形成的化合物,能与NaOH溶液反应的共有( )
①—CH3②—OH③—C6H5④—CHO⑤—COOH
| A.3种 | B.4种 | C.5种 | D.6种 |
下列叙述错误的是
| A.合金材料中可能含有非金属元素 |
| B.人造纤维,合成纤维和光导纤维都是有机高分子化合物 |
| C.加热能杀死流感病毒是因为病毒的蛋白质受热变性 |
| D.在汽车排气管上加装“催化转化器”是为了减少有害气体的排放 |
某气态烃与氧气的混合气体在密闭容器中完全燃烧,燃烧前后容器内压强相等且温度都保持在150℃。该烃不可能是()
| A.CH4 | B.C2H4 | C.C3H4 | D.C3H6 |
取11.2 g铁粉和4.8 g硫粉均匀混合加热至红热,冷却后加足量盐酸,在标准状况下能收集到的气体体积为( )
| A.4.48 L | B.3.36 L | C.2.24 L | D.1.12 L |
已知S、Cr两元素的最高价均为+6,则下列粒子中,从化合价分析,可能存在过氧键(—O—O—)的是( )
A.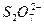 |
B.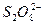 |
C.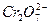 |
D.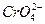 |