烧杯中盛有下列物质,敞口放置一段时间后,溶液质量会增加的是
| A.浓盐酸 | B.浓硫酸 | C.浓硝酸 | D.浓醋酸 |
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
A. mol·L-1 mol·L-1 |
B.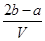 mol·L-1 mol·L-1 |
C.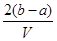 mol·L-1 mol·L-1 |
D.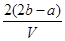 mol·L-1 mol·L-1 |
某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+,将溶液滴在蓝色石蕊试纸上,试纸变红。取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀。下列判断合理的是
| A.一定有Cl- | B.一定有SO42- |
| C.一定没有Al3+ | D.一定没有CO32- |
在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
| A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 |
| B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- |
| C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
| D.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO |
由14CO和12CO组成的混合气体与同温同压下空气的密度相等(空气的平均相对分子质量为29),则下列关系正确的是
| A.混合气体中,12CO占有的体积等于14CO占有的体积 |
| B.混合气体中,12CO与14CO分子个数之比为1∶2 |
| C.混合气体中,12CO与14CO质量之比为15∶14 |
| D.混合气体中,12CO与14CO密度之比为14∶15 |
下列指定反应的离子方程式正确的是
| A.Cu溶于稀HNO3:Cu+ 2H++ NO3-=Cu2+ + NO2↑+ H2O |
| B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2+ + 2OH-=Fe(OH)2↓ |
| C.用CH3COOH溶解CaCO3:CaCO3 + 2H+=Ca2+ + H2O+ CO2↑ |
| D.向NaAlO2溶液中通过量CO2制Al(OH)3:CO2+ AlO2-+ 2H2O =Al(OH)3↓+ HCO3- |