某兴趣小组的同学为探究实验室久置的氢氧化钠固体的成分,进行了有关实验,请你与他们完成以下探究:
【提出猜想】猜想I:全部是氢氧化钠;猜想II:全部是碳酸钠;猜想III:_________________。
【实验验证】
(1)请完成猜想III;
(2)溶液1中加足量稀盐酸,产生无色、无味的气体,说明原固体中含有_________;
(3)溶液2中滴加过量BaCl2溶液的目的是____________________________,反应的化学方程式为 。
(4)由以上实验现象可知猜想_______正确;
(5)久置的NaOH固体变质的原因是(用化学方程式表示)____________________。
某学校实验小组的同学,在实验室里将稀硫酸和氯化钡溶液混合后,发现产生白色沉淀,他们将反应后的溶液进行过滤,得到滤液,滤液中溶质的成分是什么呢?于是他们进行了如下探究.
【提出问题】反应后滤液中溶质的成分是什么?
【猜想与假设】端端同学认为反应后滤液中的溶质是HCl
默默同学认为反应后滤液中的溶质是HCl、H2SO4
硕硕同学认为反应后滤液中的溶质是H2SO4和BaCl2
【探究与交流】(1)请说出端端同学猜想的理由_________________;
(2)上述哪位同学的猜想不正确;请说明理由_________________;
(3)默默同学为了证明自己的猜想,向反应后的滤液中加入几滴石蕊溶液,紫色石蕊溶液变红,于是认为自己猜想正确,请对他的结论进行评价_________________.
(4)经过同学们多次实验证明端端、默默的猜想都是错误的,滤液中的溶质应该是_________________.
达州盛产天然气,有“中国气都”之称的美誉。天然气的主要成分是甲烷(CH4),我校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
【猜想与假设】
甲 CO2 H2O ;乙 CO H2O;
丙 NH3CO2 H2O;丁 CO2 CO H2O 。
你认为同学的猜想是错误的,理由是。
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置: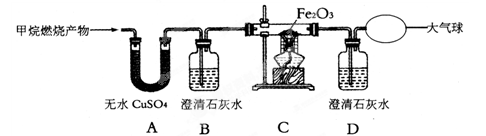
A、B装置的顺序能否颠倒?(填“能"或“否”)。
实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断同学猜想成立。
请写出C中硬质玻璃管内发生反应的化学方程式:。
小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬。好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加。
【作出猜想】
猜想1.Cr>Fe>Cu;猜想2. Fe>Cu >Cr;猜想3.你的猜想是。
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
【结论与解释】
(1)小聪得到的结论是猜想正确。
(2)实验前用砂纸打磨金属片的目的是。
【知识运用】
将铬片投入FeSO4溶液中,反应(填“能”或“不能”)进行。若能进行,
请你写出反应的化学方程式。
小华同学配制50g溶质质量分数为20%的NaCl溶液,操作流程如图:
(1)小华同学应称取氯化钠的质量是g,量取水体积为mL
(2)指出图中的一处错误:
(3)在用托盘天平称取食盐的过程中,发现指针已偏向分度盘左侧,他接下来的操作是
(4)如果小华配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能原因有(填序号)。
A.称量前天平没有调平
B.称量纸上残留少量食盐
C.向烧杯中加水时,有少量水溅出烧杯外
明星化学兴趣小组就空气中氧气的含量进行实验探究.
【集体讨论】
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应,而且生成物为固体。他们应该选择(填编号).
| A.蜡烛 | B.红磷 | C.硫粉 | D.光亮的铁丝 |
为了充分消耗容器中的氧气,药品的用量应保证.
(2)小组同学共同设计了如下图的两套装置,你认为合理的是(填编号).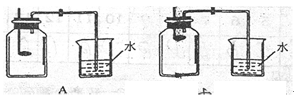
为了确保实验的成功,在装药品之前应该.
【分组实验】
在讨论的基础上,他们分组进行了实验.
【数据分析】
实验结束后,整理数据见下表.(注:集气瓶容积为100 mL)
| 组别 |
1 |
2 |
3 |
4 |
5 |
6 |
| 进入集气瓶中水的体积(mL) |
20 |
21 |
19 |
20 |
22 |
18 |
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的.通过实验还可推断集气瓶中剩余气体的性质是.