已知A~E是初中化学的常见物质。A和D是两种常见的碱;B是一种常见的酸,且只含有两种元素;C是一种钠盐。它们相互间转化或发生反应的关系如图所示。(“—”表示两种物质间能发生反应,“→”表示两种物质间的转化关系)请回答:
(1)B的化学式是 ,C的化学式是 。
(2)C→E发生的反应,属于 反应(填基本反应类型)
(3)C与D反应的化学方程式是 。
右图是已破损的维生素C(简写为Vc)片剂说明书的部分信息。已知维生素C由碳、氢、氧三种元素组成。请回答。
(1)Vc中碳、氢元素的质量比为 。
(2)Vc的化学式为 。
(3)小辉的妈妈每天服用该Vc片,小辉建议他妈妈可食用西红柿来代替Vc片,若100 g西红柿含Vc 30 mg,则小辉的妈妈每天食用西红柿 g即可达到服用上述Vc片的效果
下图是化学实验中常用的几种装置。
请回答下列问题:
(1)指出有编号的仪器名称:① ,② 。
(2)利用上述A、B装置的组合制取氧气,写出该反应的化学反应方程式 。
(3)若用E装置干燥生成的氧气,E中还应试盛放的液体试剂是 ,气体应从 端导入(填“a”或“b”)。
(4)F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是 植物油上方原有的空气对实验的结果 (填“有”或“没有”)明显影响。
(5)写出用石灰石和稀盐酸制取二氧化碳的化学方程式 ,可选用图中 和_________(填标号)组装一套制取二氧化碳的装置。检验二氧化碳的方法是 。
某金属冶炼厂的管道烟泥中含有炭黑及金属铜和锌。综合实践活动小组的同学设计了从管道烟泥中回收金属铜的实验方案,实验过程如图所示:
请回答:
(1)步骤①中,过滤操作使用了玻璃棒,其作用是 ;在过滤时,实践活动小组的同学发现过滤速度很慢,原因可能是 (填一种可能的情况)。滤液B中的溶质有 (填一种)。
(2)步骤④中,所加入的金属X是当今世界上产量最高用途最广泛的金属,该反应的化学方程式是____________________
(3)除去不纯铜中的杂质金属X,可选用的试剂有 (填一种)。
(4)在进行“反应①”“反应③”“反应④”操作时,可将反应物加入 中(填仪器名称),然后_______________(填操作名称),使反应充分进行。
(1)自热米饭是一种快餐食品。请根据图及表信息,回答下列问题:
| 营养素 |
每份含量 |
| 油脂 |
23.5g |
| 糖类 |
104.7g |
| 维生素 |
3.5g |
| 钠 |
814mg |
| 钙 |
130mg |
| 水 |
小于210g |
①从表中“自热米饭的营养成分”看,没有标出的人体必须的营养素是 。
②上述包装材料一般是符合卫生标准的铝箔。铝可以压制成铝箔,说明铝具有良好的 。
③该自热米饭是利用发热包中的生石灰与水反应放出热量来进行加热,生石灰与水反应的化学方程式为 。
(2)良好的家居环境带来美好的生活。
①房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲醛、苯等有毒气体,这是利用活性炭的 性。
②如图,“火立熄”是一种新型的家用灭火用品。“火立熄”接触到火焰3-5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使火焰熄灭。“火立熄”的灭火原理
是 (填字母标号)。
A.清除可燃物 B. 使燃烧物与氧气隔绝 C.降低燃烧物的着火点
空气、水、燃料是人类赖以生存的自然资源。
(1)人类时刻都离不开空气,是因为空气中的氧气能
(2)为了保护环境,用煤作燃料的煤炉要适当增加进风口,将煤粉吹起使之剧烈燃烧,请解释这种做法有利于节能的原因是 。
(3)自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示: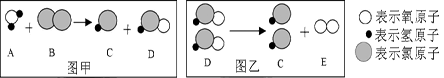
图乙所示反应的基本类型为 ;
写出图甲所示反应的化学方程式 。