下表是有机物A、B的有关信息。
| A |
B |
| ①能使溴的四氯化碳溶液退色 ②比例模型为:  ③能与水在一定条件下反应生成醇 |
①由C、H两种元素组成 ②球棍模型为: 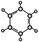 |
根据表中信息回答下列问题:
(1)A的名称为___________,A在一定条件下生成高分子化合物的反应方程式________________。
(2)A与氢气发生加成反应后生成分子C,C在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n= 时,这类有机物开始出现同分异构体。
(3)B具有的性质是 (填序号)。
①无色无味液体、②有毒、③不溶于水、④密度比水大、
⑤与酸性KMnO4溶液和溴水反应使之退色、⑥任何条件下不与氢气反应。
(4)写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:_____________________________。
组成一种原电池如图所示。试回答下列问题(灯泡功率合适):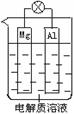
(1)电解质溶液为稀H2SO4时,灯泡______(填“亮”做①题,填“不亮”做②题) 。
。
①若灯泡亮,则Mg电极上发生的反应为:____________________;
Al电极上发生的反应为:___________________________________。
②若灯泡不亮,其理由为:__________________________________。
(2)电解质溶液为NaOH溶液时,灯泡_____(填“亮”做①题,填“不亮”做②题)。
①若灯泡亮,则Al电极上发生的反应为:_____________________________。
②若灯泡不亮,其理由为:__________________________________________。
已知A是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。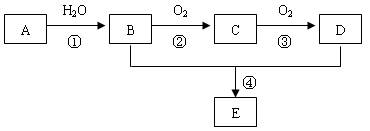
请回答下列问题:
(1)写出A的结构简式。
(2)B、D分子中的官能团名称分别是、。
(3)物质B可以被直接氧化为D,需要加入的试剂是。
(4)写出下列反应的化学方程式:
①;反应类型:。
④。反应类型:。
某烷烃的蒸气质量是相同条件下氢气质量的36倍,该烃的分子式为____________,写出该烃同分异构体的结构简式:
在盛有少量无水乙醇的试管中,加入一小块新切的、擦干表面煤油的金属钠,迅速用配有导管的单孔塞塞住试管口,用一小试管收集并验纯气体后,点燃,并把干燥的小烧杯罩在火焰上,,片刻,迅速倒转烧杯,向烧杯中加入少量澄清石灰水。观察现象,完成下表。
| 乙醇与钠反应的现象 |
气体燃烧的现象 |
检验产物 |
| 气体燃烧时火焰呈, 小烧杯内壁, 澄清石灰水。 |
反应中只生成了 |
写出乙醇与钠反应的化学方程式
已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个石油化工发展水平的标志。下列是有机物A~G之间的转化关系: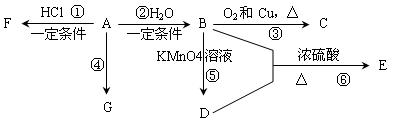
请回答下列问题:
(1)A的官能团的名称是________________;C的结构简式是________________;
(2)E是一种具有香味的液体,由B + D→的反应方程式为:___________________________________,该反应类型是_______________;
如何除去E中所混有少量的D杂质,简述操作过程:________________________________________
______________________________________________________________________________________;
(3)G是一种高分子化合物,其名称是_____________,链节是______________;
(4)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F(沸点12.27OC)进行应急处理。写出由A制F的化学反应方程式:________________________________,该反应的原子利用率为__________,决定F能用于冷冻麻醉应急处理的性质是________________________________
__________________________________________。