氮的固定是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值。
| 反应 |
大气固氮 N2 (g)+O2 (g)  2NO(g) 2NO(g) |
工业固氮 N2 (g)+3H2 (g)  2NH3(g) 2NH3(g) |
|||
| 温度/℃ |
27 |
2000 |
25[ |
400 |
450 |
| K |
3.84×10-31 |
0.1 |
5×108 |
0.507 |
0.152 |
①分析数据可知:大气固氮反应属于__________(填“吸热”或“放热”)反应。
②分析数据可知:人类不适合大规模模拟大气固氮的原因__________。
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因_______________________。
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,下图所示的图示中,正确的是______(填“A”或“B”);比较р1、р2的大小关系_______。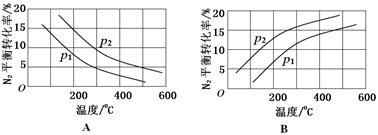
(3)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(1) 4NH3(g)+3O2(g),则其反应热ΔH=___________________。
4NH3(g)+3O2(g),则其反应热ΔH=___________________。
(已知:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ·mol-1
2NH3(g) △H=-92.4kJ·mol-1
2H2(g) +O2(g) 2H2O(l) △H=-571.6kJ·mol-1 )
2H2O(l) △H=-571.6kJ·mol-1 )
小艾同学在妈妈买回的某食品包装内发现有一包白色颗粒状固体A的小纸袋,上面写着“生石灰干燥剂,请勿食用”。小艾同学随手将小纸袋放在窗台上,过一段时间后发现纸袋内的白色颗粒粘在一起成为块状固体B。小艾同学请你和同学们一起对块状固体B进行探究。
(1)猜想一:块状固体B中除氧化钙外,还可能有(写两种);
(2)猜想二:块状固体B溶于水可能有现象(填“放热”或“吸热”)。
(3)取块状固体B加入盛有一定量水的试管内,振荡、静置、过滤,得到少量白色固体C。就白色固体C同学们展开了热烈讨价,一起猜想。
小艾同学认为白色固体C可能是氢氧化钙,小聪同学认为白色固体C可能是碳酸钙;你认为白色固体C还可能是(任写一种)。
世界是物质的,物质是由各种化学元素组成的,请你写出下列物质的化学式:
(1)“西气东输”工程中输送的气体是;
(2)水银不是银,是一种金属的俗称,这种金属是;
(3)既可用来消毒杀菌,又可用来改良酸性土壤的碱是;
(4)氧元素的质量分数最多的氧化物是。
某校实验小组的同学用实验的方法区别稀盐酸和稀硫酸钠溶液(记作M、N),请你一同参与。
⑴甲组同学向M、N中分别加入少量的铁粉,观察到M中产生大量无色气泡,则M中发生反应的化学方程式为。
⑵乙组同学向M、N中分别滴加Na2CO3溶液,发现M也有无色气泡产生,N没有气泡产生,则M中发生反应的化学反应方程式为。
⑶丙组同学向M、N中分别加入滴加BaCl2溶液,N中出现的现象是。
⑷丁组同学用了下列试剂中的一种也将M、N区别开来,这种试剂是(填序号)
①酚酞试液②硫酸铜溶液③氯化钠溶液④pH试纸
A、B、C、D都是初中化学中的常见物质,具有如图所示的转化关系(反应条件、有些反应物或产物已略去):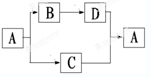
(1)若A是一种白色难溶于水的钙盐,由三种元素组成,C 是大气循环循环中的一种重要物质.则B的化学式是 ,C和D反应生成A的化学方程式是 。
(2)若A是无色液体,D是一种黑色固体.则C的化学式是 ,由B生成D的化学方程式为 。
(3)若A是碳酸氢钠,且已知碳酸氢钠受热可分解为碳酸钠、二氧化碳和水.写出过量的气体C与D溶液反应生成A的化学方程式 。
如右图所示,弹簧秤下挂着一重物A,烧杯中盛有溶液B,试根据要求回答下列问题: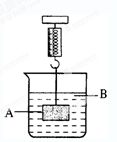
(1)若A为铝块,B为稀硫酸,将A放入B中,过一会儿,弹簧秤的读数将(填“变大”“变小”或“不变”),反应的化学方程式为。
(2)若A为铁块,B为硫酸铜溶液,将A放入B中,过一会儿,弹簧秤的读数将(填 “变大”“变小”或“不变”),反应的化学方程式为。